Energie Vitalité Santé Naturellement
Comprendre les liens possibles entre infections parasitaires et processus tumoraux

Pourquoi s’intéresser au lien parasites–cancer ?
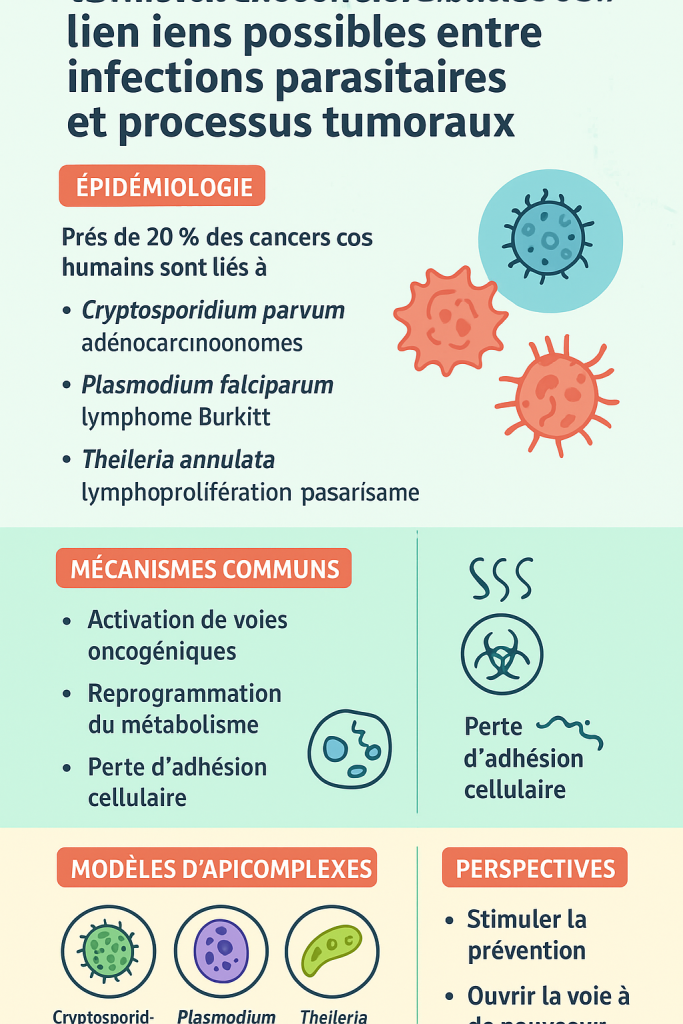
Bien que le cancer soit une maladie multifactorielle impliquant gènes, environnement et mode de vie, on estime que près de 20 % des cancers humains dans le monde sont liés à des infections.
Les virus (HPV, HBV, EBV) et certaines bactéries (H. pylori) sont des causes reconnues depuis plusieurs décennies… mais le rôle potentiel des parasites eucaryotes, notamment les apicomplexes, reste largement méconnu du grand public.
Pourtant, plusieurs études — dont celle publiée dans Médecine/Sciences (2016, Cheeseman, Certad & Weitzman) — montrent que certains parasites intracellulaires manipulent profondément la cellule hôte, d’une manière étonnamment proche des mécanismes de la cellule cancéreuse.
1. Parasites et cancer : ce que dit l’épidémiologie
Les agents infectieux reconnus comme cancérogènes
L’IARC répertorie déjà 11 agents infectieux cancérogènes, dont :
- Schistosoma haematobium → cancer de la vessie
- Opisthorchis viverrini → cholangiocarcinome
Mais les apicomplexes, parasites intracellulaires, pourraient aussi être impliqués.
Parasites suspectés d’un rôle oncogène
1) Cryptosporidium parvum
- Modèles animaux : apparition d’adénocarcinomes digestifs chez les souris SCID.
- Études chez l’humain : signaux préoccupants, surtout en cas d’infection chronique.
2) Plasmodium falciparum
- Forte corrélation géographique entre paludisme chronique et lymphome de Burkitt chez l’enfant.
- L’effet serait indirect : activation excessive des lymphocytes B + co-infection EBV.
3) Theileria annulata (bétail)
- Transforme littéralement les leucocytes en cellules se comportant comme des cellules tumorales.
- Constitue un modèle unique d’oncogenèse parasitaire.
2. Comment un parasite pourrait-il favoriser un cancer ?
Les parasites intracellulaires vivent au cœur de la cellule, et pour survivre, ils détournent sa machinerie.
Ce détournement ressemble de façon frappante à la transformation cancéreuse.
a) Activation de voies oncogéniques
Certains parasites stabilisent ou activent des gènes ou protéines impliqués dans le cancer :
- c-Myc (prolifération cellulaire)
- β-caténine / voie Wnt (transition épithélio-mésenchymateuse)
- BCL-2 (anti-apoptose)
- p53 (gène suppresseur de tumeur)
b) Reprogrammation du métabolisme (effet Warburg)
Comme les cellules tumorales, les cellules infectées par certains parasites augmentent leur glycolyse, modifient leur respiration mitochondriale et stabilisent HIF-1α, promoteur classique de la croissance tumorale.
c) Perte d’adhésion cellulaire et invasion
Cryptosporidium altère :
- l’E-cadhérine
- les jonctions serrées
- l’organisation du cytosquelette
Ces modifications rappellent la transition vers un phénotype invasif, caractéristique des cancers avancés.
d) Induction d’instabilité génomique
Le paludisme augmente l’expression d’AID (Activation-Induced Deaminase), une enzyme pouvant provoquer :
- mutations somatiques,
- cassures double brin,
- translocations,
notamment celles caractéristiques du lymphome de Burkitt.
3. Les trois parasites modèles qui éclairent l’oncogenèse infectieuse
3.1 Cryptosporidium parvum : un suspect majeur du cancer digestif
- Provoque des adénocarcinomes dans les modèles murins immunodéprimés.
- Altère profondément les voies APC/β-caténine, p53 et BCL-2.
- Favorise une perte d’adhésion et une prolifération anarchique des cellules intestinales.
3.2 Plasmodium falciparum : le pont vers le lymphome de Burkitt
Le parasite :
- stimule excessivement les centres germinatifs B,
- favorise une expansion clonale,
- induit l’enzyme AID responsable de translocations oncogéniques,
particulièrement en présence du virus EBV.
3.3 Theileria annulata : un parasite qui « transforme » les cellules
Chez les bovins, Theileria :
- infecte les leucocytes,
- les fait proliférer à l’infini,
- active des modules oncogéniques comme TaPIN-1 → c-JUN → miR-155,
- provoque l’équivalent d’un lymphome.
C’est un modèle expérimental exceptionnel pour comprendre comment un parasite peut pousser une cellule vers un phénotype tumoral.
4. Ce que ces découvertes signifient pour l’avenir
✔ Stimuler la prévention
Si certaines infections parasitaires influencent le risque de cancer, de nouvelles stratégies de santé publique pourraient émerger :
- contrôle de l’eau contaminée,
- vaccination contre le paludisme,
- détection et traitement des infections chroniques.
✔ Ouvrir la voie à de nouveaux traitements
Les manipulations moléculaires exercées par ces parasites pourraient devenir des cibles thérapeutiques inédites contre certains cancers.
✔ Mieux comprendre la biologie tumorale
Les parasites fournissent des modèles naturels pour observer la transformation cellulaire en temps réel.
Conclusion
Bien que les parasites ne soient pas encore officiellement classés parmi les causes majeures de cancer humain, les preuves s’accumulent :
✔ ils altèrent profondément les voies cellulaires clés ;
✔ certains favorisent l’instabilité génomique ;
✔ plusieurs modèles animaux montrent une progression tumorale.
Les parasites intracellulaires comme Cryptosporidium, Plasmodium et Theileria constituent aujourd’hui une piste sérieuse pour comprendre — et peut-être prévenir — certains cas de cancer encore inexpliqués.
Source : inserm
Fenbendazole : antiparasitaire vétérinaire et pistes anticancer (état des lieux)
Fenbendazole : antiparasitaire vétérinaire, pistes anticancer et précautions
Introduction
Le fenbendazole (FBZ) est un benzimidazole anthelminthique largement utilisé en médecine vétérinaire pour traiter divers helminthes et protozoaires.
Récemment, il a suscité un fort intérêt pour un repositionnement en oncologie après plusieurs études précliniques et rapports en phase de découverte du grand public.
Dans cet article, nous synthétisons l’état des connaissances, expliquons les mécanismes proposés, évaluons la qualité des preuves humaines et rappelons les précautions essentielles. ScienceDirect+1

Qu’est-ce que le fenbendazole ?
- Classe chimique : benzimidazole (famille des carbamates).
- Usage principal : traitement des parasites gastro-intestinaux chez animaux (ovins, bovins, chiens, chats). Il inhibe la polymérisation des microtubules parasitaires et bloque l’absorption du glucose chez les helminthes.
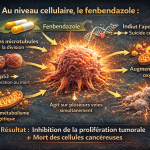
Mécanismes biologiques plausibles liés à un effet anticancer
Les études en laboratoire identifient plusieurs mécanismes par lesquels le fenbendazole pourrait affecter des cellules tumorales :
- Interaction avec la tubuline / microtubules — FBZ se lie à la β-tubuline et perturbe la polymérisation microtubulaire, entraînant l’arrêt du cycle cellulaire et l’apoptose chez des lignées tumorales in vitro. PMC
- Altération du métabolisme tumoral — des données suggèrent une inhibition du transport du glucose et une perturbation métabolique (phénotype proche de l’effet Warburg) chez certaines cellules cancéreuses. MDPI
- Induction de stress et de mort cellulaire — apoptosis, pyroptose ou autres formes de mort cellulaire ont été rapportées selon le type cellulaire et la concentration. Frontiers
Ces mécanismes coïncident avec des cibles classiques de chimiothérapie (microtubules) et expliquent pourquoi le Fenbendazole attire l’attention pour le repositionnement. PMC
Preuves expérimentales et cliniques : où en sommes-nous ?
- In vitro / in vivo (animaux) : plusieurs travaux montrent une cytotoxicité sur lignées tumorales humaines et une activité antitumorale dans des modèles animaux. Ces résultats sont encourageants mais préliminaires. PMC+1
- Séries de cas / rapports : des séries de cas et communications (y compris publications récentes) décrivent des patients ayant pris le Fenbendazole en contexte d’auto-traitement et rapportent des améliorations anecdotiques — mais ces rapports manquent souvent de témoins, de contrôles et d’informations pharmacocinétiques/posologiques fiables. Karger Publishers
- Essais cliniques : à la date actuelle, il manque des essais randomisés, de grande ampleur, validant l’efficacité et la sécurité du Fenbendazole en oncologie humaine. Des auteurs et groupes de recherche appellent à des études cliniques rigoureuses. euclid.int
Sécurité, réglementation et risques
- Statut réglementaire : FBZ est un médicament vétérinaire ; il n’est pas approuvé pour un usage humain dans la plupart des juridictions. Les agences vétérinaires européennes et autorités alimentaires donnent des informations de sécurité et de limites d’usage. European Medicines Agency (EMA)
- Effets indésirables rapportés : en médecine animale, effets digestifs, et rares complications hépatiques ou cytopénies en cas d’usage prolongé inapproprié. Chez l’humain, des cas sévères d’insuffisance hépatique ont été décrits après auto-médication en surdosage de plus de 1000mg, conduisant à hospitalisations et, dans des cas médiatisés, à des issues fatales. Ces événements rappellent le danger de l’emploi hors AMM et sans surveillance médicale.
- Interactions et pharmacocinétique : métabolisme hépatique (oxfendazole comme métabolite), faible biodisponibilité orale chez certaines espèces — paramètres pharmacocinétiques humains insuffisamment caractérisés, ce qui complique la transposition des doses animales aux humains, même si des témoignages commencent à affiner le dosage humain. Dosage humain connu. European Medicines Agency (EMA)
Recommandations pratiques & éthiques
- Ne pas recommander l’auto-médication : si l’usage humain est déconseillé en dehors d’essais cliniques encadrés, cela ne permet pas de négliger les témoignages du monde entier. Les risques hépatiques et d’interactions sont réels et l’adjonction de Chardon-Marie, acide salicylique ou Extrait d’artichaud sont préconisés avec de bon résultat pour favoriser et aider le foie . The Sun
- Favoriser la recherche clinique : soutenir la réalisation d’essais contrôlés pour déterminer si le Fenbendazole (ou dérivés) présente un rapport bénéfice/risque positif en oncologie humaine, définir posologie, formulation, profil pharmacocinétique et effets indésirables. euclid.int
- Informer et combattre la désinformation : expliquer clairement la différence entre données précliniques prometteuses et preuves cliniques robustes ; signaler les dangers des traitements non informés ou approximatifs. PMC
Conclusion
Le fenbendazole est une molécule d’intérêt pour la recherche en oncologie grâce à ses mécanismes d’action (microtubules, métabolisme) et à des résultats précliniques encourageants.
Toutefois, l’absence d’essais cliniques solides et les risques cliniques observés en cas d’usage non encadré interdisent toute recommandation grand public aujourd’hui. Les recherches doivent se poursuivre dans un cadre réglementaire et éthique strict. PMC+2euclid.int+2
Références clés
- Dogra N. et al., Fenbendazole acts as a moderate microtubule depolymerizing agent in mammalian cells, PMC (2018). PMC
- Nguyen J. et al., Oral Fenbendazole for Cancer Therapy in Humans and …, IIAR (2024). ar.iiarjournals.org
- Makis W., Fenbendazole as an Anticancer Agent? A Case Series, Cro (2025). Karger Publishers
- Lei X. et al., Fenbendazole Exhibits Antitumor Activity Against Cervical …, MDPI (2025). MDPI
- EMA / rapports sur benzimidazoles et usage vétérinaire. European Medicines Agency (EMA)
Pour savoir où se procurer du Fenbendazole de qualité, cliquez l’image ci-dessous :