Energie Vitalité Santé Naturellement
L’ivermectine, la recherche et le cancer (suite)
Posted on mai 31, 2026 by BienEtreNaturel
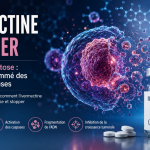
7. Comment l’ivermectine pourrait-elle provoquer la mort des cellules cancéreuses ?
L’un des aspects les plus fascinants des recherches sur l’ivermectine concerne sa capacité potentielle à déclencher différents mécanismes de mort cellulaire programmée.
Contrairement à une cellule saine, une cellule cancéreuse développe souvent des stratégies lui permettant d’échapper aux signaux naturels qui devraient normalement conduire à sa destruction.
L’objectif de nombreux traitements anticancéreux consiste précisément à réactiver ces mécanismes d’autodestruction.
Selon les études publiées à ce jour, l’ivermectine pourrait agir sur trois formes principales de mort cellulaire :
- l’apoptose ;
- l’autophagie ;
- la pyroptose.
Chacune de ces voies possède ses propres caractéristiques biologiques et pourrait jouer un rôle différent selon le type de cancer concerné.
7.1. L’apoptose : le suicide programmé de la cellule cancéreuse
L’apoptose est souvent décrite comme un suicide cellulaire organisé.
Il s’agit d’un mécanisme naturel indispensable à la survie de l’organisme.
Chaque jour, des milliards de cellules vieillissantes, endommagées ou inutiles sont éliminées grâce à ce processus.
Chez les personnes atteintes de cancer, ce système est fréquemment perturbé.
Les cellules tumorales apprennent progressivement à contourner ces signaux de destruction, ce qui leur permet de survivre beaucoup plus longtemps que prévu.
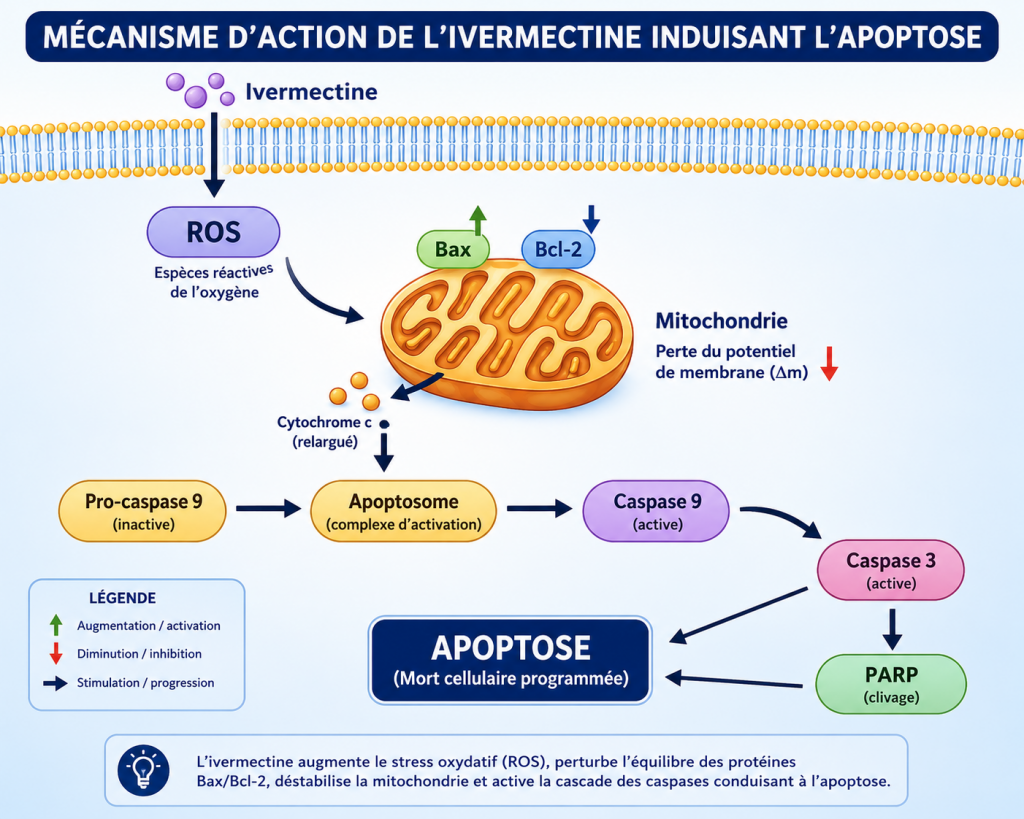
Comment l’ivermectine déclenche-t-elle l’apoptose ?
Les études montrent que l’ivermectine agit principalement au niveau des mitochondries.
Comme nous l’avons vu précédemment, les mitochondries sont les centrales énergétiques de la cellule.
Lorsqu’elles sont perturbées, elles peuvent déclencher une cascade d’événements conduisant à la mort cellulaire.
Après exposition à l’ivermectine, les chercheurs ont observé :
- une diminution du potentiel membranaire mitochondrial ;
- une altération de la production d’énergie ;
- une libération du cytochrome c ;
- une activation des enzymes appelées caspases.
Ces événements constituent les étapes classiques de l’apoptose mitochondriale.
Le rôle des protéines Bax et Bcl-2
Deux protéines jouent un rôle particulièrement important :
Bax : la protéine qui favorise la mort cellulaire
Lorsque son expression augmente :
- les mitochondries deviennent plus perméables ;
- les signaux d’apoptose sont amplifiés ;
- la cellule s’oriente vers son autodestruction.
Bcl-2 : la protéine protectrice
À l’inverse, Bcl-2 protège la cellule contre l’apoptose.
Dans de nombreux cancers, cette protéine est anormalement élevée.
Les chercheurs ont observé que l’ivermectine :
- augmente l’expression de Bax ;
- diminue l’expression de Bcl-2.
Ce double effet favorise fortement l’apoptose.
Activation des caspases
Les caspases sont parfois surnommées les « exécuteurs » de la cellule.
Une fois activées, elles découpent progressivement les structures internes de la cellule cancéreuse.
L’ivermectine active notamment :
- la caspase-9 ;
- la caspase-3.
Ces enzymes provoquent ensuite :
- la fragmentation de l’ADN ;
- la condensation du noyau ;
- la destruction progressive de la cellule.
Dans quels cancers ce mécanisme a-t-il été observé ?
L’apoptose induite par l’ivermectine a été observée dans :
- le cancer du col de l’utérus ;
- le cancer colorectal ;
- le cancer du poumon ;
- le mélanome ;
- le glioblastome ;
- les leucémies ;
- le cholangiocarcinome ;
- plusieurs cancers du sein.
Ces observations expliquent pourquoi l’apoptose est aujourd’hui considérée comme le principal mécanisme anticancéreux associé à l’ivermectine.
7.2. L’autophagie : lorsque la cellule se recycle jusqu’à s’épuiser
L’autophagie signifie littéralement « se manger soi-même ».
Il s’agit d’un mécanisme naturel de nettoyage cellulaire.
La cellule recycle en permanence :
- ses protéines usées ;
- ses organites endommagés ;
- ses déchets métaboliques.
Dans des conditions normales, ce système contribue à maintenir l’équilibre cellulaire.
Un mécanisme à double visage
L’autophagie possède une particularité importante :
elle peut parfois aider les cellules cancéreuses à survivre.
En période de stress ou de manque de nutriments, les cellules tumorales utilisent l’autophagie comme système de secours énergétique.
Cependant, lorsque ce mécanisme devient excessif, il peut produire l’effet inverse et conduire à la mort cellulaire.
C’est précisément ce phénomène que les chercheurs ont observé avec l’ivermectine.
L’autophagie induite par l’ivermectine
Dans plusieurs cancers, notamment :
- le cancer du sein ;
- le mélanome ;
- certains gliomes ;
l’ivermectine provoque une augmentation importante de l’activité autophagique.
Les chercheurs ont observé :
- une accumulation d’autophagosomes ;
- une augmentation de LC3 ;
- une augmentation de Beclin-1 ;
- une augmentation d’Atg5.
Ces protéines sont considérées comme des marqueurs majeurs de l’autophagie.
La voie Akt/mTOR : une cible centrale
La voie Akt/mTOR agit normalement comme un frein de l’autophagie.
Lorsqu’elle est fortement activée :
- la croissance cellulaire augmente ;
- l’autophagie diminue ;
- la survie tumorale est favorisée.
L’ivermectine semble inhiber cette voie.
Cette inhibition libère alors les mécanismes autophagiques et favorise l’autodestruction progressive de la cellule cancéreuse.
Des preuves expérimentales solides
Les chercheurs ont utilisé des inhibiteurs de l’autophagie afin de vérifier cette hypothèse.
Lorsque l’autophagie était bloquée :
- l’efficacité anticancéreuse de l’ivermectine diminuait fortement ;
- la destruction des cellules devenait moins importante.
Ces résultats suggèrent que l’autophagie participe activement à l’effet antitumoral observé.
7.3. Apoptose et autophagie : une relation complexe
Pendant longtemps, les scientifiques ont considéré l’apoptose et l’autophagie comme deux mécanismes totalement indépendants.
Les recherches récentes montrent qu’ils sont en réalité étroitement liés.
Deux mécanismes qui s’influencent mutuellement
Selon le contexte biologique :
- l’autophagie peut protéger contre l’apoptose ;
- l’autophagie peut favoriser l’apoptose ;
- l’apoptose peut bloquer l’autophagie.
Cette interaction dépend :
- du type de cancer ;
- du stade tumoral ;
- du niveau de stress cellulaire ;
- du microenvironnement tumoral.
L’exemple du mélanome
Dans certaines cellules de mélanome, les chercheurs ont observé que l’autophagie protégeait partiellement les cellules contre l’apoptose induite par l’ivermectine.
Lorsque l’autophagie était bloquée :
- l’apoptose augmentait fortement.
L’exemple du cancer du sein
À l’inverse, dans certains modèles de cancer du sein, une augmentation de l’autophagie semblait renforcer l’effet anticancéreux global de l’ivermectine.
Ces observations montrent que la relation entre ces deux mécanismes reste complexe et probablement spécifique à chaque type de cancer.
7.4. La pyroptose : une forme explosive de mort cellulaire
La pyroptose est beaucoup moins connue que l’apoptose.
Pourtant, elle suscite aujourd’hui un intérêt croissant en oncologie.
Contrairement à l’apoptose, qui est relativement silencieuse, la pyroptose déclenche une réponse inflammatoire importante.
Comment fonctionne la pyroptose ?
Lorsqu’une cellule entre en pyroptose :
- elle gonfle rapidement ;
- sa membrane se perce ;
- son contenu est libéré dans l’environnement ;
- des signaux inflammatoires sont activés.
Cette réaction peut attirer des cellules immunitaires capables d’attaquer la tumeur.
Le rôle des inflammasomes
La pyroptose repose sur l’activation de structures appelées inflammasomes.
Ces complexes moléculaires activent ensuite :
- la caspase-1 ;
- plusieurs cytokines inflammatoires ;
- différentes protéines impliquées dans la destruction cellulaire.
Ce que montrent les études sur l’ivermectine
Dans certaines cellules de cancer du sein, les chercheurs ont observé :
- une activation de la caspase-1 ;
- une augmentation de la libération de LDH ;
- un gonflement cellulaire ;
- une rupture membranaire.
Ces phénomènes sont compatibles avec une pyroptose.
Les chercheurs pensent que la voie :
P2X4 → P2X7 → NLRP3
pourrait jouer un rôle important dans ce mécanisme.
Cependant, les preuves restent encore limitées et des recherches supplémentaires sont nécessaires.
Ce qu’il faut retenir
Les données expérimentales suggèrent que l’ivermectine pourrait combattre les cellules cancéreuses en activant plusieurs programmes biologiques de destruction :
L’apoptose
Le mécanisme actuellement le mieux documenté.
Il repose principalement sur les mitochondries, les protéines Bax/Bcl-2 et les caspases.
L’autophagie
Un système de recyclage cellulaire qui, lorsqu’il devient excessif, peut conduire à la mort des cellules tumorales.
La pyroptose
Une forme de mort inflammatoire plus récente, encore en cours d’étude, qui pourrait contribuer à stimuler la réponse immunitaire antitumorale.
L’un des enseignements majeurs de ces recherches est que l’ivermectine ne semble pas agir par un seul mécanisme, mais par plusieurs voies complémentaires. Cette capacité à cibler simultanément différents processus biologiques pourrait expliquer l’intérêt croissant qu’elle suscite dans la recherche sur le repositionnement des médicaments anticancéreux.
mectine
1.2. 3. L’ivermectine contre le cancer : que révèlent les recherches scientifiques ?
4.L’ivermectine dans les cancers du système urinaire et les cancers du sang
5.Ivermectine et cancers gynecologiques
6.L’ivermectine dans les cancers respiratoires et le mélanome
7.Comment l’ivermectine pourrait-elle provoquer la mort des cellules cancéreuses ?
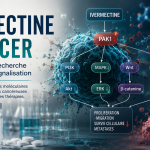
9.PAK1 et les voies de signalisation : le cœur du mécanisme anticancéreux potentiel de l’ivermectine
10.L’ivermectine contre le cancer : où en est réellement la science en 2026 ?
Source de l’article : https://pmc.ncbi.nlm.nih.gov/articles/PMC7505114/
Lire la suite >>>>
L’ivermectine, le cancer et la recherche scientifique (suite)
Posted on mai 31, 2026 by BienEtreNaturel
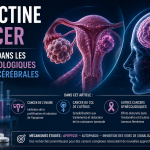
5. L’ivermectine dans les cancers gynécologiques et les tumeurs cérébrales
Parmi les nombreuses recherches consacrées à l’ivermectine, plusieurs études ont exploré son potentiel dans les cancers gynécologiques et certaines tumeurs du système nerveux central.
Ces cancers présentent souvent des caractéristiques particulières : agressivité élevée, résistance aux traitements, risque important de récidive et options thérapeutiques parfois limitées.
Les résultats obtenus en laboratoire montrent que l’ivermectine pourrait agir sur plusieurs mécanismes impliqués dans leur développement, notamment le cycle cellulaire, l’apoptose, l’autophagie, l’angiogenèse et certaines voies de signalisation essentielles à la survie tumorale.
5.1. Cancer du col de l’utérus : blocage de la prolifération et induction de l’apoptose
Le cancer du col de l’utérus demeure l’un des cancers féminins les plus fréquents dans le monde.
Chaque année, plusieurs centaines de milliers de nouveaux cas sont diagnostiqués, principalement en lien avec une infection persistante par certains papillomavirus humains (HPV).
Un effet observé sur les cellules HeLa
Les chercheurs ont étudié l’action de l’ivermectine sur les célèbres cellules HeLa, utilisées depuis des décennies dans la recherche biomédicale.
Après exposition à l’ivermectine, plusieurs phénomènes ont été observés :
- diminution de la prolifération cellulaire ;
- ralentissement de la migration tumorale ;
- augmentation de la mort programmée des cellules ;
- altération du cycle cellulaire.
Un blocage du cycle cellulaire
Avant de se diviser, une cellule doit franchir plusieurs étapes de contrôle.
Les chercheurs ont constaté que l’ivermectine bloquait les cellules cancéreuses à la transition G1/S.
Cette étape est cruciale puisqu’elle marque l’engagement irréversible de la cellule vers la division.
En empêchant ce passage, l’ivermectine freine directement la multiplication tumorale.
Des signes caractéristiques d’apoptose
Les cellules traitées présentaient également plusieurs marqueurs typiques d’apoptose :
- condensation du noyau ;
- fragmentation de l’ADN ;
- rétrécissement cellulaire ;
- formation de corps apoptotiques.
Ces observations indiquent que l’ivermectine ne se contente pas de ralentir la croissance tumorale : elle peut également déclencher l’autodestruction des cellules cancéreuses.
5.2. Cancer de l’ovaire : une cible thérapeutique particulièrement intéressante
Le cancer de l’ovaire est souvent diagnostiqué tardivement car ses symptômes initiaux sont peu spécifiques.
Cette caractéristique explique en partie son taux de mortalité relativement élevé.
Une inhibition de la kinase PAK1
Plusieurs études ont montré que l’ivermectine ralentissait la croissance de différentes lignées cellulaires de cancer ovarien.
L’un des mécanismes majeurs identifiés concerne la protéine PAK1.
Cette kinase joue un rôle essentiel dans :
- la prolifération cellulaire ;
- la migration tumorale ;
- l’invasion des tissus ;
- la résistance aux traitements.
Lorsque PAK1 est inhibée, la cellule cancéreuse perd une partie de sa capacité d’adaptation et de survie.
Une action sur la protéine KPNB1
Les chercheurs ont également identifié une autre cible potentielle : KPNB1.
Cette protéine intervient dans le transport de nombreuses molécules entre le cytoplasme et le noyau.
Dans plusieurs cancers, une surexpression de KPNB1 favorise :
- la prolifération tumorale ;
- la survie cellulaire ;
- la progression de la maladie.
L’ivermectine semble perturber cette voie, entraînant :
- un blocage du cycle cellulaire ;
- une augmentation de l’apoptose ;
- une réduction de la croissance tumorale.
Une amélioration de l’efficacité du paclitaxel
Le paclitaxel constitue l’un des traitements de référence du cancer de l’ovaire.
Les expériences réalisées chez l’animal ont montré qu’une association entre l’ivermectine et le paclitaxel produisait un effet antitumoral supérieur à celui obtenu avec chacun des traitements utilisés séparément.
Cette observation suggère un potentiel effet synergique.
Une meilleure réponse au cisplatine
Le cisplatine reste également une chimiothérapie majeure dans le traitement des cancers gynécologiques.
Selon plusieurs travaux, l’ivermectine pourrait renforcer son efficacité en inhibant la voie Akt/mTOR.
Cette voie est souvent impliquée dans :
- la survie des cellules tumorales ;
- la résistance aux traitements ;
- la progression du cancer.
Son inhibition pourrait rendre les cellules plus sensibles aux agents anticancéreux.
5.3. Gliomes et glioblastomes : une activité intéressante mais des limites importantes
Les gliomes sont les tumeurs cérébrales primitives les plus fréquentes.
Parmi eux, le glioblastome représente la forme la plus agressive.
Malgré la chirurgie, la radiothérapie et la chimiothérapie, le pronostic demeure souvent défavorable.
Une inhibition de la croissance tumorale
Les chercheurs ont observé que l’ivermectine ralentissait la prolifération de plusieurs lignées cellulaires de glioblastome.
L’effet était proportionnel à la dose administrée.
Plus la concentration augmentait, plus la croissance tumorale diminuait.
Une apoptose dépendante des caspases
Comme dans plusieurs autres cancers, l’ivermectine semble déclencher l’apoptose.
Cette action repose notamment sur l’activation des caspases, enzymes spécialisées dans l’exécution du programme de mort cellulaire.
Les cellules exposées présentent :
- une fragmentation nucléaire ;
- une dégradation de l’ADN ;
- une altération des mitochondries ;
- une disparition progressive de leur activité métabolique.
Le rôle du stress oxydatif
Les chercheurs ont également constaté une augmentation importante des espèces réactives de l’oxygène (ROS).
Lorsque leur concentration devient excessive, les cellules cancéreuses ne parviennent plus à maintenir leur équilibre interne.
Cette accumulation favorise alors l’apoptose.
Une inhibition de l’angiogenèse
Pour se développer, une tumeur doit construire son propre réseau vasculaire.
Ce processus est appelé angiogenèse.
L’ivermectine semble capable d’inhiber cette étape en provoquant l’apoptose de certaines cellules endothéliales impliquées dans la formation des vaisseaux sanguins.
Cette propriété pourrait théoriquement :
- limiter l’alimentation de la tumeur ;
- ralentir sa croissance ;
- réduire le risque de dissémination.
Une action sur la voie Akt/mTOR
Comme dans le cancer du sein ou de l’ovaire, l’ivermectine semble également inhiber la voie Akt/mTOR dans certaines cellules de gliome.
Cette voie constitue l’un des principaux moteurs biologiques de nombreuses tumeurs.
Son inhibition pourrait contribuer à :
- ralentir la prolifération ;
- favoriser l’autophagie ;
- augmenter la sensibilité aux traitements.
Le rôle potentiel de DDX23
Des travaux récents ont également suggéré que l’ivermectine pourrait agir sur une hélicase à ARN appelée DDX23.
Cette protéine participe à la régulation de plusieurs microARN impliqués dans :
- la prolifération tumorale ;
- l’invasion ;
- les métastases.
En perturbant cette voie, l’ivermectine pourrait réduire certains comportements agressifs des cellules tumorales.
Une limite majeure : la barrière hémato-encéphalique
Malgré ces résultats encourageants, un obstacle important demeure.
L’ivermectine franchit difficilement la barrière hémato-encéphalique.
Cette barrière protège naturellement le cerveau en empêchant de nombreuses molécules présentes dans le sang d’y pénétrer.
Par conséquent, même si l’ivermectine montre une activité intéressante sur les cellules tumorales cérébrales en laboratoire, atteindre des concentrations efficaces dans le cerveau humain reste aujourd’hui un défi majeur.
C’est probablement l’une des raisons pour lesquelles son application clinique dans les gliomes demeure encore très hypothétique.
Ce qu’il faut retenir
Les études précliniques suggèrent que l’ivermectine pourrait :
- ralentir la croissance du cancer du col de l’utérus ;
- favoriser l’apoptose des cellules tumorales ;
- inhiber la kinase PAK1 dans le cancer de l’ovaire ;
- renforcer l’efficacité du paclitaxel et du cisplatine ;
- réduire la prolifération des gliomes ;
- limiter l’angiogenèse tumorale ;
- agir sur plusieurs voies de signalisation majeures comme Akt/mTOR.
Cependant, dans le cas des tumeurs cérébrales, la faible pénétration de l’ivermectine à travers la barrière hémato-encéphalique constitue aujourd’hui une limitation importante qui devra être surmontée avant d’envisager une utilisation clinique.
mectine
1.2. 3. L’ivermectine contre le cancer : que révèlent les recherches scientifiques ?
4.L’ivermectine dans les cancers du système urinaire et les cancers du sang
5.Ivermectine et cancers gynecologiques
6.L’ivermectine dans les cancers respiratoires et le mélanome
7.Comment l’ivermectine pourrait-elle provoquer la mort des cellules cancéreuses ?
9.PAK1 et les voies de signalisation : le cœur du mécanisme anticancéreux potentiel de l’ivermectine
10.L’ivermectine contre le cancer : où en est réellement la science en 2026 ?
Source de l’article : https://pmc.ncbi.nlm.nih.gov/articles/PMC7505114/
Lire la suite >>>>
L’ivermectine contre le cancer et recherches scientifiques
Posted on mai 31, 2026 by BienEtreNaturel
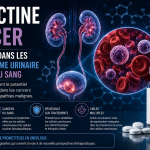
4. L’ivermectine dans les cancers du système urinaire et les cancers du sang (suite)
Les recherches sur l’ivermectine ne se limitent pas aux cancers digestifs ou au cancer du sein. Plusieurs études expérimentales ont également exploré son potentiel dans les cancers du rein, de la prostate et dans certaines leucémies.
Même si ces travaux restent principalement réalisés en laboratoire ou chez l’animal, ils apportent des informations intéressantes sur les mécanismes biologiques que pourrait cibler cette molécule.
4.1. Cancer du rein : une action ciblant les mitochondries
Le carcinome à cellules rénales est la forme la plus fréquente de cancer du rein chez l’adulte.
Son incidence continue d’augmenter dans de nombreux pays et certaines formes avancées répondent encore difficilement aux traitements disponibles.
Une inhibition sélective des cellules cancéreuses
Des chercheurs ont étudié l’effet de l’ivermectine sur plusieurs lignées cellulaires de cancer du rein.
Les résultats ont montré que la molécule ralentissait fortement la croissance des cellules cancéreuses tout en épargnant largement les cellules rénales normales.
Cette sélectivité est particulièrement intéressante car elle représente l’un des objectifs majeurs de la recherche en cancérologie : détruire les cellules tumorales tout en limitant les dommages sur les tissus sains.
Un dysfonctionnement énergétique des cellules tumorales
Les travaux réalisés suggèrent que l’ivermectine agit notamment sur les mitochondries.
Les mitochondries sont souvent décrites comme les « centrales énergétiques » des cellules.
Après exposition à l’ivermectine, les chercheurs ont observé :
- une diminution du potentiel membranaire mitochondrial ;
- une baisse de la production d’énergie cellulaire ;
- une réduction de la synthèse d’ATP ;
- une augmentation du stress oxydatif.
Privées d’énergie, les cellules cancéreuses deviennent progressivement incapables de maintenir leurs fonctions vitales.
Des expériences complémentaires ont montré que certains nutriments et antioxydants pouvaient atténuer ces effets, renforçant l’hypothèse d’un mécanisme centré sur le métabolisme mitochondrial.
Des résultats confirmés chez l’animal
Dans les modèles animaux, les tumeurs traitées présentaient des marqueurs élevés de stress mitochondrial.
Cette observation confirme que les effets observés en laboratoire pourraient également se produire dans un organisme vivant.
4.2. Cancer de la prostate : un potentiel pour améliorer certaines hormonothérapies
Le cancer de la prostate est l’un des cancers masculins les plus fréquents dans les pays occidentaux.
Même si les traitements hormonaux ont considérablement amélioré la prise en charge de la maladie, la résistance thérapeutique demeure un problème majeur.
Une amélioration de l’efficacité de l’enzalutamide
Des chercheurs ont découvert que l’ivermectine pouvait renforcer l’action de l’enzalutamide, un médicament utilisé contre les formes avancées de cancer de la prostate.
L’association des deux traitements semblait produire un effet supérieur à celui obtenu avec l’enzalutamide seul.
Une réduction des résistances au traitement
Les résultats les plus intéressants concernent probablement les cellules devenues résistantes au docétaxel, une chimiothérapie fréquemment utilisée dans le cancer de la prostate métastatique.
Les études ont montré que l’ivermectine pouvait restaurer partiellement la sensibilité de ces cellules au traitement.
Ce phénomène est particulièrement important car la résistance aux médicaments constitue l’une des principales causes d’échec thérapeutique.
Une activité directe sur les cellules tumorales
Au-delà de son rôle d’adjuvant, l’ivermectine semble également capable de ralentir directement la croissance de certaines lignées cellulaires prostatiques.
Ces observations renforcent l’idée que cette molécule pourrait agir simultanément sur plusieurs mécanismes impliqués dans la progression tumorale.
4.3. Les leucémies : une sensibilité particulière à l’ivermectine
Les leucémies sont des cancers qui prennent naissance dans les cellules responsables de la fabrication du sang.
Contrairement aux tumeurs solides, elles se développent principalement dans la moelle osseuse et circulent dans le sang.
Une destruction préférentielle des cellules leucémiques
Lors d’études de criblage de médicaments anticancéreux, les chercheurs ont observé que l’ivermectine était capable de tuer certaines cellules leucémiques à des concentrations relativement faibles.
Fait particulièrement intéressant : les cellules sanguines normales semblaient beaucoup moins affectées.
Cette différence de sensibilité pourrait constituer un avantage potentiel dans le développement de futurs traitements.
Une augmentation du stress oxydatif
Le mécanisme observé implique plusieurs phénomènes :
- augmentation de l’entrée des ions chlorure dans la cellule ;
- modification du potentiel électrique membranaire ;
- production accrue de radicaux libres (ROS) ;
- stress oxydatif important ;
- activation des voies de mort cellulaire.
Lorsque ce stress devient trop important, la cellule cancéreuse déclenche son propre programme d’autodestruction.
Des effets renforcés en association avec la chimiothérapie
Les chercheurs ont également observé un effet synergique avec plusieurs médicaments utilisés dans les leucémies, notamment :
- la cytarabine ;
- la daunorubicine.
Cette synergie signifie que les médicaments semblent agir plus efficacement lorsqu’ils sont utilisés ensemble.
Leucémie myéloïde chronique : une action sur les mitochondries
Dans les cellules de leucémie myéloïde chronique (LMC), l’ivermectine a provoqué :
- un dysfonctionnement mitochondrial ;
- une augmentation du stress oxydatif ;
- une activation des caspases ;
- une augmentation de l’apoptose.
Les chercheurs ont également observé que le dasatinib, une thérapie ciblée utilisée dans la LMC, devenait plus efficace lorsqu’il était associé à l’ivermectine.
Ce qu’il faut retenir
Les données expérimentales montrent que l’ivermectine pourrait agir contre plusieurs cancers du système urinaire et du sang en :
- perturbant le métabolisme énergétique des cellules tumorales ;
- ciblant les mitochondries ;
- augmentant le stress oxydatif ;
- favorisant l’apoptose ;
- améliorant l’efficacité de certains traitements existants ;
- réduisant certaines formes de résistance thérapeutique.
Les résultats les plus encourageants concernent actuellement :
- le carcinome à cellules rénales ;
- le cancer de la prostate ;
- la leucémie myéloïde chronique ;
- plusieurs autres formes de leucémies étudiées en laboratoire.
Comme pour les autres cancers abordés précédemment, ces observations restent essentiellement précliniques et nécessitent encore une validation par des essais cliniques rigoureux avant toute utilisation en pratique médicale.
mectine
1.2. 3. L’ivermectine contre le cancer : que révèlent les recherches scientifiques ?
4.L’ivermectine dans les cancers du système urinaire et les cancers du sang
5.Ivermectine et cancers gynecologiques
6.L’ivermectine dans les cancers respiratoires et le mélanome
7.Comment l’ivermectine pourrait-elle provoquer la mort des cellules cancéreuses ?
9.PAK1 et les voies de signalisation : le cœur du mécanisme anticancéreux potentiel de l’ivermectine
10.L’ivermectine contre le cancer : où en est réellement la science en 2026 ?
Source de l’article : https://pmc.ncbi.nlm.nih.gov/articles/PMC7505114/
Lire la suite >>>>
Le cancer, fenbendazole & Phyto Oncologie
Posted on mai 4, 2026 by BienEtreNaturel

Plantes et cancer : curcumine, berbérine… protocole naturel efficace
Et si le cancer ne se traitait pas avec une seule solution ?
Pendant des années, la recherche a tenté d’isoler LA molécule miracle capable de vaincre le cancer.
Résultat ?
Des milliers d’études, des milliers de pistes… mais aucune solution unique.
La réalité est plus complexe :
le cancer n’est pas une maladie unique, mais un déséquilibre global.
Et c’est précisément là que les approches naturelles prennent tout leur sens.
Le vrai défi : traiter sans détruire
Les traitements conventionnels, notamment la chimiothérapie, reposent sur un principe simple :
- détruire les cellules cancéreuses
- sans compromettre la survie du patient
Mais dans les faits, cet équilibre est fragile.
C’est ici que certaines molécules issues des plantes changent la donne :
- elles renforcent l’efficacité des traitements
- elles limitent les effets secondaires
- elles agissent sur le terrain biologique profond
Pourquoi les plantes sont au cœur de la stratégie anticancer ?
Les plantes ne peuvent ni fuir, ni se défendre physiquement.
Elles ont donc développé au fil de l’évolution une chimie extrêmement sophistiquée :
- molécules anti-inflammatoires
- antioxydants puissants
- régulateurs hormonaux
- modulateurs du microbiote
Ces composés agissent en synergie, là où la médecine conventionnelle agit souvent de manière ciblée.
Les 6 molécules naturelles incontournables contre le cancer
1. Curcumine : le chef d’orchestre anti-cancer

Extraite du curcuma, la curcumine est l’une des molécules les plus étudiées au monde.
Actions principales
- bloque la prolifération des cellules cancéreuses
- favorise leur destruction naturelle (apoptose)
- inhibe les mécanismes de résistance aux traitements
- régule l’inflammation et le stress oxydatif
Ce que dit la science
Plus de 1800 publications montrent son intérêt en prévention et en accompagnement thérapeutique.
Posologie recommandée
- 2 à 10 g par jour
- sous forme biodisponible (avec pipérine ou lipides)
2. Berbérine : le régulateur métabolique majeur

La berbérine agit directement sur le terrain biologique du cancer.
Effets clés
- régulation du microbiote
- réduction de l’inflammation
- amélioration de la sensibilité à l’insuline
- inhibition de la croissance tumorale
Pourquoi elle est essentielle
La majorité des patients présentent un terrain inflammatoire et métabolique déséquilibré.
Posologie
- 500 mg minimum par jour
- forme hautement assimilable indispensable
3. Acide bétulinique : l’anti-tumeur du bouleau

Issu de l’écorce de bouleau, ce composé est encore peu connu mais extrêmement prometteur.
Actions
- inhibition de la prolifération tumorale
- induction de la mort cellulaire
- blocage de l’angiogenèse (vascularisation tumorale)
Posologie
- 100 à 500 mg par jour selon les extraits
4. Tocotriénols : la vraie vitamine E anticancer

Contrairement aux idées reçues, la vitamine E ne se limite pas aux tocophérols.
Les tocotriénols, notamment le gamma, sont les plus actifs.
Effets
- inhibition des cellules souches cancéreuses
- réduction des métastases
- régulation de l’inflammation
Posologie
- 100 à 300 mg par jour (origine annatto)
5. Génistéine : régulation hormonale intelligente

Issue du soja, la génistéine est souvent mal comprise.
Réalité scientifique
Elle n’augmente pas le risque hormonal :
elle agit comme un régulateur.
Actions
- inhibition des voies de croissance tumorale
- effet anti-angiogénique
- modulation des récepteurs œstrogéniques
Posologie
- 30 à 100 mg par jour
6. Lycopène : l’arme secrète de la tomate

Le lycopène est un caroténoïde puissant… mais mal utilisé.
Clé essentielle
Il est beaucoup plus efficace cuit avec une matière grasse
Effets
- réduction du stress oxydatif
- inhibition de la prolifération tumorale
- protection contre plusieurs cancers (prostate, poumon, digestif)
Conseil pratique
- consommer régulièrement de la sauce tomate avec huile d’olive
Le facteur clé oublié : le microbiote
Aujourd’hui, la science est formelle :
Le microbiote contrôle :
- l’immunité
- l’inflammation
- la réponse aux traitements
Un microbiote déséquilibré favorise :
- la progression tumorale
- la résistance thérapeutique
Le détail qui change tout : la mastication
Cela peut sembler basique… mais c’est fondamental.
Sans mastication efficace :
- digestion incomplète
- nutriments mal absorbés
- microbiote déséquilibré
Règle simple
Mastiquer jusqu’à obtenir une texture quasi liquide.
Les 6 piliers d’un terrain anti-cancer

Pour optimiser votre stratégie, il est essentiel de surveiller : (accédez aux fournisseurs si vous le voulez via les liens ci-dessous )
- Inflammation → CRP ultrasensible → Test sanguin de votre état inflammatoire & équilibrage
- Glycémie → éviter l’hyperinsulinisme → Test Glycémique et recommandations informatives
- Stress oxydatif → Curcumine → Berbérine
- Vitamine D → idéalement 60 à 80 ng/ml → Test sanguin & Vitamine D optimisée
- Microbiote Intestinal → Test Sanguin et rééquilibrage de votre microbiote
- Déparasitage → Fenbendazole – Mebendazole – Ivermectine
7. L’action incroyable du Fenbendazole
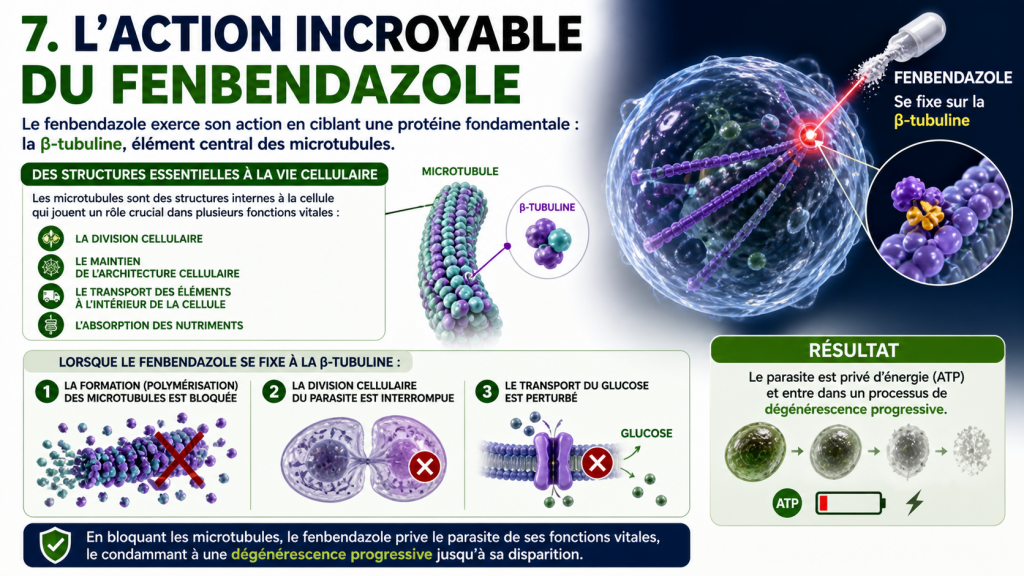
Le fenbendazole exerce son action en ciblant une protéine fondamentale : la β-tubuline, élément central des microtubules.
Ces structures internes à la cellule jouent un rôle crucial dans plusieurs fonctions vitales :
- la division cellulaire
- le maintien de l’architecture cellulaire
- le transport des éléments à l’intérieur de la cellule
- l’absorption des nutriments
Lorsque le fenbendazole se fixe à la β-tubuline :
- la formation (polymérisation) des microtubules est bloquée
- la division cellulaire du parasite est interrompue
- le transport du glucose est perturbé
Conséquence directe : privé de ses ressources énergétiques (ATP), le parasite entre progressivement dans un processus de dégénérescence, jusqu’à sa disparition.
Conclusion : changer de paradigme
Le cancer ne se résume pas à une tumeur à éliminer.
C’est un déséquilibre global qui nécessite une approche globale.
Associer :
- traitements conventionnels
- nutrition adaptée
- molécules naturelles
- hygiène de vie
➡️ C’est aujourd’hui l’approche la plus cohérente, la plus logique… et probablement la plus efficace.

CURCUMINE | BERBERINE | ACIDE BETULINIQUE |VIT E – TOCOTRIENOLS | GENISTEINE | FENBENDAZOLE
Important
Cet article est informatif. Toute stratégie doit être encadrée par un professionnel de santé qualifié.
Fenbendazole et cancer du sein : un potentiel anticancéreux
Posted on avril 29, 2026 by BienEtreNaturel
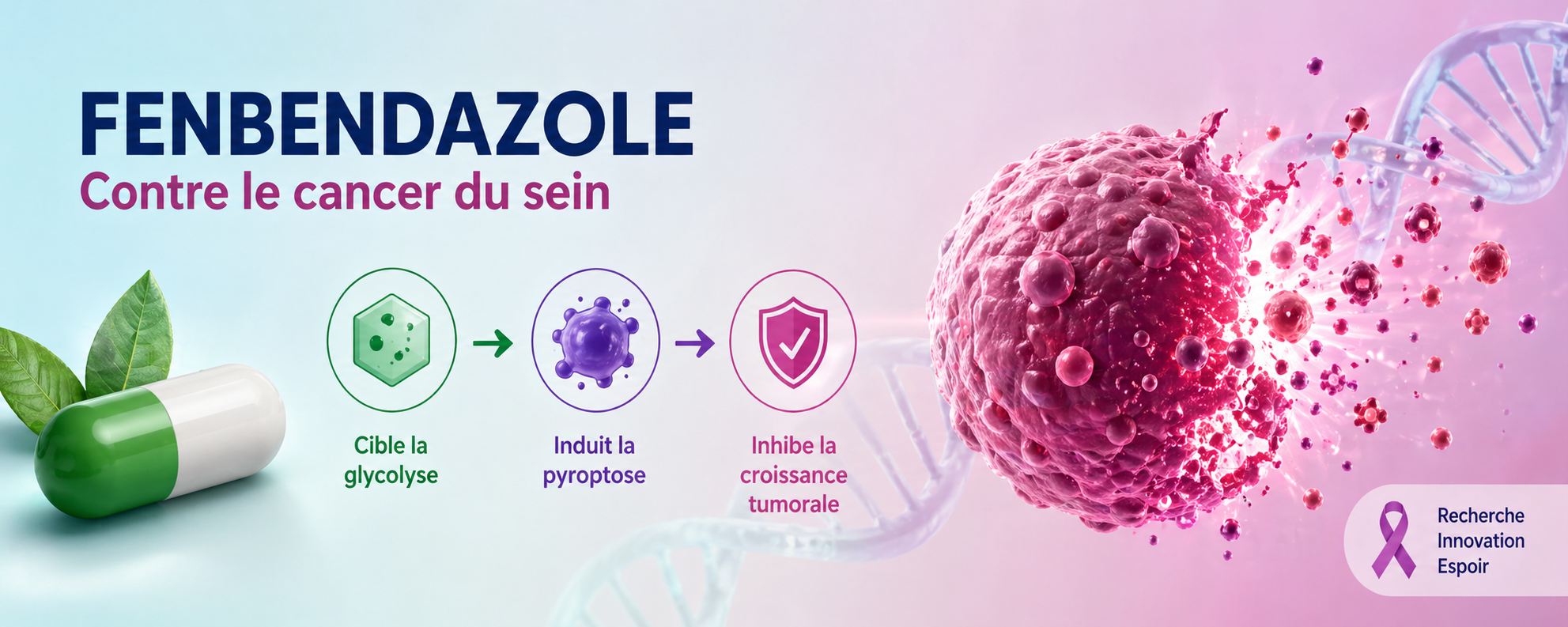
Fenbendazole et cancer du sein : un potentiel anticancéreux via la pyroptose et la glycolyse
Une nouvelle piste face à la résistance thérapeutique
Le traitement du cancer du sein reste un défi majeur en oncologie moderne. L’une des principales difficultés réside dans la capacité des cellules tumorales à développer des mécanismes complexes de résistance aux traitements conventionnels (Will et al., 2023).
Dans ce contexte, de nouvelles stratégies émergent, notamment autour de la pyroptose, une forme récente de mort cellulaire programmée à fort potentiel thérapeutique (Chen et al., 2022).
Parallèlement, le métabolisme énergétique des cellules cancéreuses, en particulier la glycolyse tumorale, joue un rôle clé dans la progression tumorale et la résistance aux antitumoraux (Aft et al., 2003).
Le fenbendazole (FBZ), connu comme antiparasitaire, suscite aujourd’hui un intérêt croissant pour ses propriétés anticancéreuses (Villar et al., 2007).
Fenbendazole : un antiparasitaire aux propriétés anticancéreuses
Initialement utilisé en médecine vétérinaire, le fenbendazole montre des effets prometteurs dans différents types de cancers.
Action sur le métabolisme tumoral
Dans le cancer du poumon non à petites cellules, le FBZ agit sur plusieurs cibles essentielles (Xu et al., 2022) :
- activation du gène suppresseur de tumeur p53
- inhibition du transporteur de glucose GLUT1
- blocage de l’enzyme hexokinase
- diminution de l’absorption du glucose par les cellules cancéreuses
Ces effets perturbent directement la glycolyse, un processus vital pour la survie des cellules tumorales.
Induction de l’apoptose
Le fenbendazole est également capable de déclencher l’apoptose (mort cellulaire programmée classique) :
- dans le cancer colorectal, via des lésions mitochondriales et la voie caspase-3/PARP (Jing et al., 2021)
- dans les cellules sensibles, via l’augmentation de p53
- dans les cellules résistantes au 5-FU, via des mécanismes indépendants de p53 impliquant le fer (Park et al., 2022)
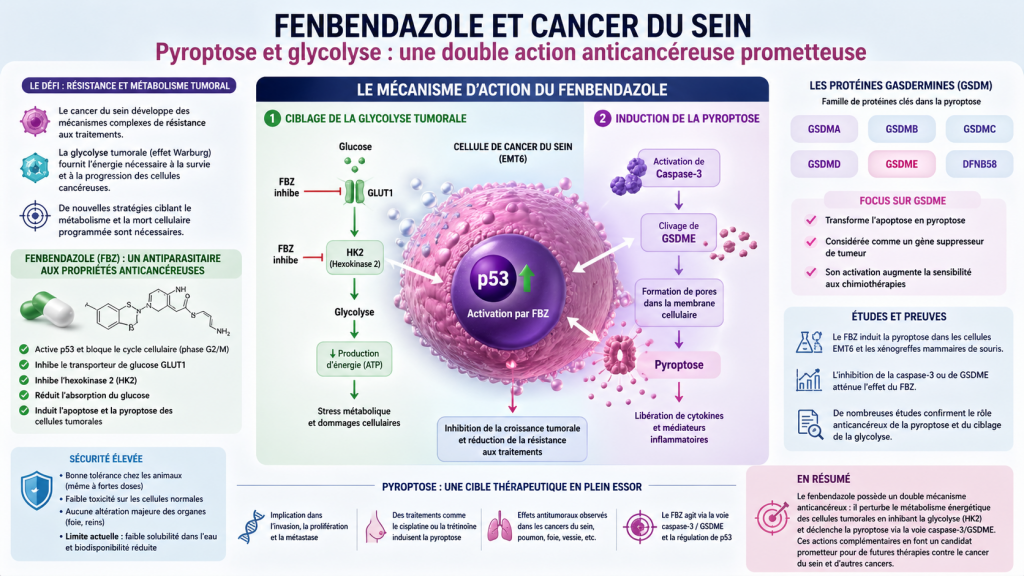
Une découverte majeure : la pyroptose induite par le fenbendazole
Des recherches récentes montrent que le FBZ ne se limite pas à l’apoptose. Il induit également la pyroptose, une forme inflammatoire de mort cellulaire.
Cette action a été observée :
- dans des cellules de cancer du sein (EMT6)
- dans des modèles animaux (xénogreffes mammaires)
Les analyses (viabilité cellulaire, imagerie tumorale, biomarqueurs) confirment clairement ce mécanisme.
Le rôle clé de la voie caspase-3 / GSDME
La pyroptose repose sur l’activation des protéines de la famille des gasdermines.
Contrairement à de nombreux traitements qui activent GSDMD, le fenbendazole agit principalement via :
la voie caspase-3 / GSDME
Pourquoi GSDME est-elle importante ?
- Elle transforme l’apoptose en pyroptose
- Elle est considérée comme un gène suppresseur de tumeur
- Son activation augmente la sensibilité aux chimiothérapies
Plusieurs études confirment son rôle clé :
- inhibition de la croissance tumorale (Lage et al., 2001)
- implication dans le cancer gastrique (Akino et al., 2007)
- conversion de l’apoptose en pyroptose sous chimiothérapie (Wang et al., 2018 ; Jung et al., 2023)
Dans cette étude, l’inhibition de caspase-3 ou de GSDME réduit fortement l’effet du FBZ, confirmant ce mécanisme.
Le rôle central du gène p53
Le gène p53 est impliqué dans plus de 50 % des cancers humains.
Il agit comme un véritable “gardien du génome” :
- blocage du cycle cellulaire
- réparation de l’ADN
- induction de l’apoptose
- inhibition de l’angiogenèse
Le fenbendazole semble stimuler l’expression de p53, renforçant ses effets anticancéreux, notamment via un blocage du cycle cellulaire en phase G2/M (Jung et al., 2023).
Glycolyse et effet Warburg : une cible thérapeutique majeure
Les cellules cancéreuses consomment massivement du glucose, même en présence d’oxygène. Ce phénomène est connu sous le nom d’effet Warburg (Zhu et al., 2022).
L’enzyme clé : HK2
L’hexokinase 2 (HK2) est essentielle à la glycolyse tumorale (Padilla et Lee, 2021).
Plusieurs composés anticancéreux ciblent déjà cette enzyme :
- xanthohumol (Liu et al., 2019)
- tanshinone IIA (Li et al., 2020)
Le fenbendazole agit également sur HK2, perturbant la glycolyse et favorisant la mort des cellules tumorales.
Sécurité et limites du fenbendazole
Un profil de sécurité favorable
Les études montrent :
- une bonne tolérance chez les animaux, même à fortes doses (Muser et Paul, 1984)
- une faible toxicité cellulaire sur les cellules normales
- aucune altération majeure des organes (foie, reins)
Une limite importante : la biodisponibilité
Le principal obstacle reste :
sa faible solubilité dans l’eau
Cela limite son absorption et son efficacité. Des recherches sont en cours pour améliorer ce point.
Pyroptose et thérapies anticancéreuses : un domaine en expansion
De nombreux traitements exploitent désormais la pyroptose :
- le cisplatine dans le cancer du sein triple négatif (Yan et al., 2021)
- la trétinoïne dans les cancers ORL (Cai et al., 2021)
Des études ont également démontré des effets antitumoraux dans :
- cancer du sein
- foie
- poumon
- vessie
(Hou et al., 2020 ; Derangère et al., 2014 ; Lin et al., 2021 ; Zhang et al., 2022)
Conclusion : un double mécanisme prometteur
Le fenbendazole apparaît comme un candidat intéressant en oncologie expérimentale grâce à une double action :
✔ inhibition du métabolisme tumoral (glycolyse via HK2)
✔ induction de la pyroptose (voie caspase-3 / GSDME)
Ces résultats ouvrent la voie à de nouvelles stratégies thérapeutiques, notamment dans les cancers résistants. Etudes sources
Commandez votre Fenbendazole de qualité pur 99% – Cliquez sur l’image ci-dessous
code coupon FENBEN10 remise de 10% immédiate

Articles récents
- Nourriture anti-cancer : les aliments qui protègent votre organisme au quotidienPeut-on réduire le risque de cancer grâce à l’alimentation ? La question revient souvent : existe-t-il une alimentation capable de prévenir le cancer ? Aucun aliment ne peut garantir à lui seul qu’une personne ne développera jamais un cancer. Cependant, les recherches scientifiques montrent...
- Ivermectine contre le cancer et la recherche10. L’ivermectine contre le cancer : où en est réellement la science en 2026 ? L’idée qu’un médicament antiparasitaire puisse devenir un traitement anticancéreux peut sembler surprenante. Pourtant, l’histoire de la médecine est remplie de découvertes similaires. De nombreuses molécules utilisées aujourd’hui contre le...
- Ivermectine, cancer, recherche et voies de signalisation9. PAK1 et les voies de signalisation : le cœur du mécanisme anticancéreux potentiel de l’ivermectine Au fil des études présentées dans cette revue scientifique, un constat revient sans cesse : malgré la diversité des cancers étudiés, plusieurs mécanismes biologiques semblent systématiquement impliqués. Cancer...
- Ivermectine, cancer, recherche et cellules souches8. Cellules souches cancéreuses, résistance aux traitements et thérapies combinées : pourquoi l’ivermectine intéresse autant les chercheurs L’une des principales difficultés en cancérologie ne consiste pas seulement à réduire la taille d’une tumeur. Le véritable défi est souvent d’empêcher son retour. De nombreux patients...
- L’ivermectine, la recherche et le cancer (suite)7. Comment l’ivermectine pourrait-elle provoquer la mort des cellules cancéreuses ? L’un des aspects les plus fascinants des recherches sur l’ivermectine concerne sa capacité potentielle à déclencher différents mécanismes de mort cellulaire programmée. Contrairement à une cellule saine, une cellule cancéreuse développe souvent des...
- Ivermectine, cancer et recherche médicale (suite)6. L’ivermectine dans les cancers respiratoires et le mélanome Les recherches sur l’ivermectine se sont également intéressées à plusieurs cancers particulièrement agressifs, notamment le cancer du poumon, le carcinome nasopharyngé et le mélanome. Ces tumeurs partagent souvent plusieurs caractéristiques communes : Les études précliniques...
- L’ivermectine, le cancer et la recherche scientifique (suite)5. L’ivermectine dans les cancers gynécologiques et les tumeurs cérébrales Parmi les nombreuses recherches consacrées à l’ivermectine, plusieurs études ont exploré son potentiel dans les cancers gynécologiques et certaines tumeurs du système nerveux central. Ces cancers présentent souvent des caractéristiques particulières : agressivité élevée,...
- L’ivermectine contre le cancer et recherches scientifiques4. L’ivermectine dans les cancers du système urinaire et les cancers du sang (suite) Les recherches sur l’ivermectine ne se limitent pas aux cancers digestifs ou au cancer du sein. Plusieurs études expérimentales ont également exploré son potentiel dans les cancers du rein, de...
- L’ivermectine contre le cancer : que révèlent les recherches scientifiques ?Résumé des principaux résultats d’une étude en 10 parties Initialement développée pour combattre les parasites, l’ivermectine suscite aujourd’hui un intérêt croissant dans le domaine de l’oncologie. Plusieurs études expérimentales montrent qu’elle pourrait agir sur différents mécanismes impliqués dans la progression tumorale. Les recherches publiées...
- Mébendazole et cancer du sein contre la chimiorésistanceMébendazole et cancer du sein : une nouvelle piste contre l’hypoxie tumorale et la chimiorésistance Longtemps utilisé comme simple antiparasitaire intestinal, le mébendazole suscite aujourd’hui un intérêt croissant dans le domaine de l’oncologie expérimentale. Cette molécule, approuvée depuis plusieurs décennies pour le traitement des...
- Fenbendazole, Mébendazole et Ivermectine contre le cancer : entre espoir, science et médecine de précisionPourquoi les médicaments antiparasitaires suscitent-ils autant d’intérêt en cancérologie ? Depuis quelques années, des médicaments autrefois réservés au traitement des parasites attirent l’attention du monde médical alternatif, intégratif et parfois même scientifique pour leurs effets potentiels contre certains cancers. Voir : Fenbendazole et cancer...
- Ivermectine et mébendazole contre le cancer : analyse de l’étude observationnelle 2026 sur 197 patientsIvermectine, mébendazole et cancer : résultats d’une cohorte observationnelle de 197 patients suivis pendant 6 mois (étude 2026) Le repositionnement thérapeutique suscite un intérêt croissant en oncologie, notamment pour des molécules anciennes dont les mécanismes biologiques pourraient dépasser leur indication d’origine. Parmi elles, l’ivermectine...
- Ivermectine, mébendazole et albendazole : activité anticancéreuse synergiqueIvermectine, mébendazole et albendazole : vers une stratégie anticancéreuse combinée contre le cancer colorectal ? L’idée d’utiliser des médicaments déjà connus pour lutter contre le cancer suscite un intérêt croissant dans le monde scientifique. Cette approche, appelée repositionnement thérapeutique, consiste à réemployer des molécules...
- Chimiothérapie : controverses et scandales médicauxChimiothérapie : controverses, scandales médicaux et remise en question d’un pilier de l’oncologie moderne Depuis plusieurs décennies, la chimiothérapie représente l’un des traitements majeurs utilisés contre le cancer aux côtés de la chirurgie, de la radiothérapie, des thérapies ciblées et plus récemment de l’immunothérapie....
- Fenbendazole & Ivermectine – Protocole métabolique inspiré du Dr William MakisProtocole métabolique inspiré du Dr William Makis : analyse scientifique, mécanismes biologiques et place potentielle des oméga-3 enrichis en polyphénols Introduction Depuis plusieurs années, certains médecins et chercheurs explorent le concept de repositionnement thérapeutique en cancérologie. Cette approche consiste à étudier des molécules déjà...
Commentaires
Archives
- juin 2026
- mai 2026
- avril 2026
- mars 2026
- février 2026
- janvier 2026
- décembre 2025
- novembre 2025
- octobre 2025
- septembre 2025
- août 2025
- juillet 2025
- mai 2025
- juillet 2023
- juin 2023
- mai 2023
- avril 2023
- mars 2023
- février 2023
- janvier 2023
- décembre 2022
- novembre 2022
- octobre 2022
- septembre 2022
- août 2022
- mai 2022
Copyright © 2026 · All Rights Reserved · Bien Etre Naturel
Theme: Natural Lite by Organic Themes · RSS Feed