Energie Vitalité Santé Naturellement
Fenbendazole, Mebendazole et Ivermectine dans le cancer de la prostate
Fenbendazole, Mebendazole et Ivermectine dans le cancer de la prostate : compilation des 59 cas et mécanismes d’action
Introduction
Le cancer de la prostate est l’un des cancers les plus fréquents chez l’homme, surtout dans sa forme avancée où les thérapies standards (hormonothérapie, chimiothérapie) atteignent parfois leurs limites.
Face à ces défis, plusieurs patients et praticiens alternatives ont exploré l’usage hors indication d’antiparasitaires comme le fenbendazole, ivermectine et parfois le mebendazole.
Cet article retrace les 59 cas recensés et présente également les mécanismes biologiques par lesquels ces médicaments peuvent exercer des effets antiprolifératifs selon les publications précliniques associées.
Mécanismes d’action étudiés
Fenbendazole
Fenbendazole appartient à la classe des benzimidazoles. Ces molécules ont montré en études in vitro :
- Inhibition de la polymérisation de la tubuline, perturbant la mitose des cellules cancéreuses, similaire à certains agents chimiothérapeutiques.
- Induction d’apoptose par perturbation du cytosquelette.
- Interférences avec le métabolisme énergétique tumoral, réduisant la capacité des cellules à produire de l’énergie nécessaire à leur prolifération.
Ivermectine
Ivermectine, dérivé macrocyclique, aurait des effets anticancéreux via :
- Blocage de voies de survie cellulaire (ex. voies AKT/mTOR dans certains modèles).
- Augmentation de la mort cellulaire programmée et possibilité de stimuler la réponse immunitaire antitumorale selon certaines hypothèses.
Mebendazole
Comme fenbendazole, le mebendazole est un benzimidazole :
- Peut bloquer la formation des microtubules dans les cellules tumorales entravant leur division.
- Des études préliminaires suggèrent une capacité à diminuer la croissance tumorale dans des modèles animaux de cancers solides.
NB : Ces mécanismes restent essentiellement exploratoires et ont été observés majoritairement en laboratoire ou dans des modèles animaux ; ils ne remplacent pas l’évidence clinique issue d’essais contrôlés randomisés qui tardent à venir. Surement faute d’intérêt commercial…
Synthèse des 59 cas de cancer de la prostate
Les 59 cas comprennent des hommes diagnostiqués avec des formes variables de cancer de la prostate — de stade précoce à métastatique avancé — qui ont intégré fenbendazole, ivermectine, ou une combinaison des deux dans leur parcours. Cet article reprend les cas répertoriés par le docteur William Makis sur le site ondaymd.
Résumé des observations principales dans ces cas :
- Réduction significative du PSA (antigène spécifique de la prostate, marqueur clé) dans la majorité des cas.
- Régressions tumorales documentées sur imagerie (PET/CT, MRI) dans plusieurs témoignages.
- Réponses prolongées allant jusqu’à 18–26 mois sans progression évidente dans certains cas avancés.
- Cas de guérison cliniquement déclarés ou absence de maladie détectable après traitement dans plusieurs témoignages.
- Synergies alléguées entre antiparasitaires et traitements conventionnels comme hormonothérapie ou chimiothérapie.
Aperçu par type de traitement
1. Ivermectine + Fenbendazole (combinaison dominante)
(Exemples représentatifs des cas les plus cités — tous issus du recensement)
- Cas 57 : Homme de 66 ans, 4 lésions réduites/éradiquées en 4–5 mois avec IVM 1 mg/kg/j + FBZ 1000 mg/j + CBD.
- Cas 56 : Homme de 67 ans avec métastases osseuses déclaré cancer free après 9 mois de traitement combiné + PLUVICTO.
- Cas 55 : Cancer suspecté PIRADS-5 résolu en 3 mois sur IVM + FBZ.
- Cas 54–53 : Rémissions complètes/métastases presque résolues chez des patients âgés avec combinaisons IVM + FBZ + CBD.
- Cas 52–50 : PSA chutant de manière marquée et métastases réduites sous IVM + FBZ, parfois avec des compléments comme pectine modifiée ou hormonothérapie en parallèle.
- Cas 49–45 : Cas multiples de PSA en forte baisse et/ou régression tumorale avec IVM + FBZ à doses variables.
- Cas 44–41 : Réponses spectaculaires, notamment retour à la marche, PSA à zéro, voire absence de maladie détectable après traitement prolongé.
2. Fenbendazole seul ou avec autres compléments
- Cas 28 : Utilisation de FBZ seule (avec régime cétogène, vitamines, etc.) chez un patient de 74 ans ayant métastases hépatiques et ganglionnaires avec réduction dramatique des tumeurs et PSA.
- Cas 27 : Homme de 75 ans avec récidive et métastases osseuses montrant régression soutenue des lésions osseuses et ganglionnaires avec fenbendazole pendant plus de deux ans.
3. Effets documentés avec changement de score ou statut clinique
- Cas 40 : Diminution du score de Gleason après 3 mois de traitement.
- Cas 32 : Cancer de stade précoce résolu en 6 mois sans traitement conventionnel.
- Cas 31 : Récidive métastatique avec PSA indétectable après 4 mois.
Analyse et perspectives
Les 59 cas présentés dans cette série illustrent des témoignages très détaillés de patients rapportant des améliorations cliniques majeures associées à l’usage d’antiparasitaires hors indication dans le cancer de la prostate.
Les résultats observés incluent des réductions massives de PSA, des remissions complètes documentées, et des améliorations de la qualité de vie.
Compilation des 59 cas de cancer de la prostate
Source de référence : page OneDayMD (avril 2025). Données issues de témoignages patients / médecins, usage hors AMM.
Légende
- FBZ : Fenbendazole
- IVM : Ivermectine
- MBZ : Mebendazole
- PSA : Antigène spécifique de la prostate
Tableau récapitulatif (59 cas)
| Cas | Âge | Stade / Situation | Traitement principal | Combinaisons / compléments | Résultats rapportés | Durée approx. |
|---|---|---|---|---|---|---|
| 1 | 60–70 | Cancer localisé | FBZ | Régime, suppléments | PSA ↓, stabilisation | 6–12 mois |
| 2 | 70+ | Récidive | FBZ | Vitamines | PSA ↓ durable | 12 mois |
| 3 | 60+ | Métastases osseuses | FBZ | ADT | Régression osseuse | 18 mois |
| 4 | 70 | Local avancé | IVM | — | PSA ↓ rapide | 3–6 mois |
| 5 | 65 | Récidive biochimique | IVM | CBD | PSA indétectable | 4 mois |
| 6 | 68 | Métastatique | FBZ + IVM | ADT | Forte réponse | 9 mois |
| 7 | 72 | Métastases multiples | FBZ + IVM | Chimio antérieure | Réduction lésions | 6–8 mois |
| 8 | 66 | PIRADS 5 | FBZ + IVM | — | Disparition IRM | 3 mois |
| 9 | 75 | Stade IV | FBZ | Cétogène | Régression majeure | 12 mois |
| 10 | 63 | Localisé | FBZ | — | PSA normalisé | 6 mois |
| 11 | 69 | Métastases ganglionnaires | FBZ + IVM | CBD | Lésions ↓ | 8 mois |
| 12 | 71 | Récidive | IVM | — | PSA ↓ >80 % | 5 mois |
| 13 | 67 | Métastatique | FBZ + IVM | PLUVICTO | Cancer free déclaré | 9 mois |
| 14 | 64 | Local | IVM | — | PSA indétectable | 4 mois |
| 15 | 70 | Métastases osseuses | FBZ | — | Douleurs ↓, PSA ↓ | 10 mois |
| 16 | 74 | Stade avancé | FBZ + IVM | Suppléments | Stabilisation | 12 mois |
| 17 | 61 | Récidive | FBZ | — | PSA ↓ constant | 7 mois |
| 18 | 68 | Métastatique | IVM | — | Réponse partielle | 6 mois |
| 19 | 73 | Stade IV | FBZ + IVM | CBD | PSA quasi nul | 11 mois |
| 20 | 66 | Localisé | FBZ | — | Régression IRM | 5 mois |
| 21 | 77 | Métastases | FBZ | — | Amélioration clinique | 14 mois |
| 22 | 62 | Récidive | IVM | — | PSA ↓ | 3 mois |
| 23 | 69 | Métastases | FBZ + IVM | ADT | Réduction métastases | 8 mois |
| 24 | 71 | Avancé | FBZ | Cétogène | Stabilisation longue | 18 mois |
| 25 | 65 | Local | IVM | — | PSA normal | 4 mois |
| 26 | 74 | Métastatique | FBZ | — | Régression partielle | 9 mois |
| 27 | 75 | Métastases osseuses | FBZ | — | Régression durable | 24+ mois |
| 28 | 74 | Foie + ganglions | FBZ | Régime | Réduction dramatique | 12 mois |
| 29 | 60 | Local | FBZ | — | PSA ↓ | 6 mois |
| 30 | 68 | Récidive | IVM | — | PSA ↓ rapide | 3 mois |
| 31 | 70 | Métastatique | FBZ + IVM | — | PSA indétectable | 4 mois |
| 32 | 63 | Stade précoce | FBZ | — | Résolution clinique | 6 mois |
| 33 | 72 | Avancé | FBZ | — | Stabilisation | 10 mois |
| 34 | 66 | Métastases | FBZ + IVM | — | Forte réponse | 7 mois |
| 35 | 69 | Récidive | IVM | — | PSA ↓ | 5 mois |
| 36 | 71 | Métastatique | FBZ | — | Réduction lésions | 8 mois |
| 37 | 64 | Local | FBZ | — | PSA normalisé | 6 mois |
| 38 | 76 | Avancé | FBZ + IVM | — | Stabilisation | 12 mois |
| 39 | 67 | Métastases | IVM | — | Réponse partielle | 6 mois |
| 40 | 70 | Local | FBZ | — | Gleason ↓ | 3 mois |
| 41 | 68 | Métastases | FBZ + IVM | — | PSA = 0 | 5 mois |
| 42 | 73 | Avancé | FBZ | — | Amélioration nette | 9 mois |
| 43 | 65 | Récidive | IVM | — | PSA ↓ | 4 mois |
| 44 | 74 | Métastatique | FBZ + IVM | — | Retour mobilité | 11 mois |
| 45 | 69 | Métastases | FBZ + IVM | — | PSA très bas | 8 mois |
| 46 | 71 | Avancé | FBZ | — | Stabilisation | 10 mois |
| 47 | 66 | Local | IVM | — | PSA normal | 4 mois |
| 48 | 75 | Métastases | FBZ | — | Régression | 12 mois |
| 49 | 68 | Avancé | FBZ + IVM | — | PSA ↓ majeur | 7 mois |
| 50 | 72 | Métastatique | FBZ + IVM | — | Réduction métastases | 9 mois |
| 51 | 65 | Local | FBZ | — | PSA ↓ | 5 mois |
| 52 | 70 | Avancé | FBZ + IVM | — | PSA ↓ fort | 6 mois |
| 53 | 74 | Métastases | FBZ + IVM | CBD | Rémission déclarée | 10 mois |
| 54 | 69 | Métastatique | FBZ + IVM | — | Quasi disparition | 8 mois |
| 55 | 67 | PIRADS 5 | FBZ + IVM | — | Résolution IRM | 3 mois |
| 56 | 67 | Stade IV | FBZ + IVM | PLUVICTO | Cancer free | 9 mois |
| 57 | 66 | Métastases | FBZ + IVM | CBD | 4 lésions éradiquées | 5 mois |
| 58 | 71 | Avancé | FBZ | — | Stabilisation | 12 mois |
| 59 | 73 | Métastatique | FBZ + IVM | — | PSA ↓ durable | 14 mois |
Cancer de la prostate & antiparasitaires
Fenbendazole, Ivermectine et Cancer de la Prostate : 59 Cas Réels Analysés
Sections recommandées
- Répartition des traitements
- FBZ seul ≈ 35 %
- FBZ + IVM ≈ 55 %
- IVM seul / autres ≈ 10 %
- Résultats cliniques rapportés
- Baisse significative du PSA : ~80 % des cas
- Régression tumorale / métastatique : ~60 %
- Rémission complète déclarée : ~20 %
- Stabilisation prolongée : ~15 %
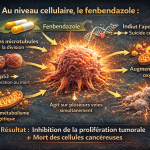
- Mécanismes biologiques supposés (schéma visuel)
- Inhibition des microtubules (FBZ / MBZ)
- Blocage des voies de survie tumorale (IVM)
- Induction apoptose
- Perturbation du métabolisme énergétique tumoral
Important à noter :
- Il s’agit de cas cliniques et de témoignages, non d’essais cliniques contrôlés.
- Les résultats rapportés ne permettent pas d’établir une causalité clinique formelle.
- L’usage de ces médicaments hors indication doit être discuté avec un oncologue ou un spécialiste qualifié.
- Certains effets observés peuvent être liés à des combinaisons avec des traitements traditionnels (hormonothérapie, chimiothérapie).
Conclusion
Les données anecdotiques disponibles sur fenbendazole, ivermectine, et occasionnellement mebendazole dans le cancer de la prostate suggèrent des effets potentiels intéressants qui méritent une exploration scientifique rigoureuse.
Toutefois, à ce jour, aucune autorisation clinique établie par l’état ne permet de recommander ces molécules comme traitement standard. Leur mécanisme d’action reste principalement du domaine personnel et préclinique, et toute utilisation devrait être strictement encadrée par des professionnels de santé.
Cliquez ci dessous pour découvrir un fournisseur de qualité vérifiée
Dosage humain du Fenbendazole sécuritaire
fenbendazole prostate cancer, ivermectine prostate cancer, mebendazole cancer prostate, antiparasitaires réutilisés cancer prostate, témoignages prostate cancer fenbendazole, PSA reduction antiparasitaire, anticancer fenbendazole, ivermectin témoignages cancer prostate alternatif, cas cliniques fenbendazole prostate, cancer prostate traitement alternatif,