Energie Vitalité Santé Naturellement
L’argent et le cancer : pourquoi le fenbendazole n’est-il pas validé par la FDA ?

Pourquoi le fenbendazole n’est-il pas approuvé contre le cancer ? Une question d’économie plus que de science
Un traitement peu coûteux face à un système coûteux
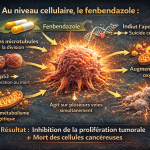
Le fenbendazole est un ancien antiparasitaire, mis au point dans les années 1970. Bon marché et disponible hors brevet, il a montré dans des études de laboratoire et sur l’animal une capacité à perturber la croissance des cellules cancéreuses. Pourtant, plus de 50 ans après son développement, il n’a jamais obtenu l’aval de la Food and Drug Administration (FDA) pour une utilisation contre le cancer.
La raison ? L’absence d’essais cliniques à grande échelle. Or, sans sponsor industriel capable d’investir près d’un milliard de dollars dans des phases successives de tests (sécurité, efficacité, comparaison à grande échelle), aucun médicament ne peut être officiellement homologué aux États-Unis.
Le débat autour du fenbendazole suscite un vif intérêt depuis quelques années. Bien que des travaux en laboratoire et sur animaux aient montré qu’il pouvait bloquer la croissance de cellules cancéreuses, ce médicament vétérinaire à bas prix n’a jamais été validé comme traitement anticancéreux par la FDA (Food and Drug Administration). La raison n’est pas uniquement scientifique, elle est aussi économique et réglementaire.
Les conditions d’approbation par la FDA
Pour obtenir la mention « anticancéreux » sur une étiquette, il faut franchir plusieurs étapes :
- Phase 1 : évaluer la tolérance sur un petit groupe de volontaires ;
- Phase 2 : mesurer l’efficacité et trouver la dose adéquate ;
- Phase 3 : comparer à grande échelle sur des centaines ou milliers de patients.
À cela s’ajoutent : inspections, études toxicologiques, et un volume considérable de dossiers réglementaires.
Le coût médian estimé pour amener un nouveau médicament sur le marché : environ 985 millions de dollars selon une étude JAMA (2020). Pour les anticancéreux, la facture grimpe souvent entre 1 et 2 milliards de dollars.
L’obstacle des brevets
Le fenbendazole est tombé dans le domaine public depuis longtemps :
- Aucun monopole possible ;
- Prix de production très bas ;
- Pas de marge permettant de facturer plusieurs milliers de dollars par mois.
Une entreprise pourrait tenter de breveter une formulation modifiée, mais les protections seraient fragiles et peu rentables. En clair, le potentiel économique est trop faible pour intéresser les grands laboratoires.
L’argent derrière l’oncologie moderne
Les médicaments contre le cancer représentent aujourd’hui l’un des marchés les plus lucratifs :
- En 2023, le coût moyen d’un nouveau traitement injectable était de 27 688 $ par mois ;
- Entre 2011 et 2022, le prix médian de lancement est passé de 32 000 $ à plus de 220 000 $ par thérapie ;
- En 2024, le seul Keytruda® (Merck) a rapporté 29,5 milliards de dollars.
Face à cela, un traitement comme le fenbendazole coûterait moins de 100 $ par mois. Inutile de dire qu’il ne fait pas rêver Wall Street.
Impact pour les patients et familles
La réalité, c’est la toxicité financière du cancer :
- 42 % des patients américains épuisent leurs économies en deux ans après le diagnostic (NCI, 2024) ;
- Beaucoup réduisent les doses, retardent les examens ou abandonnent faute de moyens.
Exemple typique : un foyer de classe moyenne doit gérer un traitement ciblé à 20 000 $ par mois. Même avec une assurance, les frais annexes (déplacements, hébergements, arrêts de travail) plongent la famille dans l’endettement.
Un traitement sûr et peu coûteux pourrait changer la donne, mais l’absence de rentabilité bloque son exploration clinique.
Les limites structurelles
- Medicaid : restrictions et autorisations préalables ralentissent l’accès aux traitements.
- Medicare : le plafond de reste à charge de 2 000 $ par an (dès 2025) reste élevé pour de nombreux retraités.
Si le fenbendazole était validé, il réduirait drastiquement ces coûts. Mais sans sponsor, il reste ignoré.
Pourquoi l’industrie ne s’y intéresse pas
- Pas de brevet exploitable.
- Trop peu cher pour générer des marges.
- Les budgets de recherche sont dirigés vers des molécules capables de rapporter plusieurs milliards par an.
En conséquence :
- Les patients perdent des alternatives.
- Les médecins manquent de données cliniques validées pour prescrire.
- La science se prive peut-être d’une molécule prometteuse.

Conclusion
Le fenbendazole n’est pas rejeté parce qu’il est inefficace, mais parce qu’il est non rentable dans le modèle actuel de développement pharmaceutique.
Pendant que les familles se battent contre la maladie et la faillite, des options abordables restent inexploitées, piégées dans un système qui valorise le profit avant le potentiel thérapeutique.
Cliquez ci dessous pour découvrir un fournisseur de qualité vérifiée