Energie Vitalité Santé Naturellement
Ivermectine : un médicament aux multiples facettes
Posted on mai 11, 2026 by BienEtreNaturel

Ivermectine : un médicament aux multiples facettes entre antiparasitaire, immunomodulation, virologie et recherche anticancéreuse
L’ivermectine est aujourd’hui considérée comme l’un des médicaments les plus marquants de la pharmacologie moderne. Découverte dans les années 1970 par le microbiologiste japonais Satoshi Omura et le parasitologue irlandais William C. Campbell, cette molécule dérivée des avermectines a profondément transformé la prise en charge des maladies parasitaires humaines et vétérinaires.
Initialement développée pour lutter contre les infections causées par les nématodes et certains arthropodes, l’ivermectine a progressivement suscité l’intérêt de la communauté scientifique pour des applications bien plus vastes. Au fil des décennies, de nombreuses recherches ont exploré ses propriétés anti-inflammatoires, antivirales, immunomodulatrices et même anticancéreuses. Cette polyvalence pharmacologique explique pourquoi l’ivermectine continue de faire l’objet d’études intensives dans différents domaines médicaux.
Origine et découverte de l’ivermectine
L’histoire de l’ivermectine débute avec l’étude d’une bactérie du sol appelée Streptomyces avermitilis. Cette bactérie produit naturellement des composés bioactifs connus sous le nom d’avermectines, capables d’agir contre de nombreux parasites.
Les travaux de Satoshi Omura au Japon permirent d’isoler plusieurs souches bactériennes prometteuses. William Campbell poursuivit ensuite les recherches en démontrant l’efficacité antiparasitaire exceptionnelle de ces molécules chez l’animal puis chez l’humain.
Commercialisée en 1981 par le laboratoire Merck Sharp and Dohme pour un usage vétérinaire, l’ivermectine fut rapidement reconnue comme une avancée thérapeutique majeure. Son efficacité spectaculaire contre l’onchocercose, également appelée « cécité des rivières », transforma la lutte contre cette maladie parasitaire qui touchait des millions de personnes dans certaines régions d’Afrique et d’Amérique latine.
Au-delà de son intérêt médical, l’ivermectine est devenue un symbole d’action humanitaire mondiale grâce aux vastes programmes de distribution destinés aux populations les plus défavorisées.
Structure chimique et mécanisme d’action antiparasitaire
L’ivermectine appartient à la famille des lactones macrocycliques. Son activité repose principalement sur sa capacité à perturber le fonctionnement neurologique des parasites.
Chez les invertébrés, l’ivermectine agit sur les canaux chlorure glutamate-dépendants présents dans les cellules nerveuses et musculaires. Cette interaction provoque une paralysie puis la mort du parasite.
La molécule agit également sur certains mécanismes de transport membranaire impliquant la glycoprotéine P. De nombreux parasites présentent une faible capacité à éliminer l’ivermectine, ce qui augmente son efficacité thérapeutique.
Cette spécificité explique pourquoi l’ivermectine possède une toxicité relativement faible chez l’humain lorsqu’elle est utilisée aux doses recommandées.
Les principales indications antiparasitaires de l’ivermectine
Aujourd’hui, l’ivermectine est utilisée contre un large éventail d’infections parasitaires humaines.
Elle intervient notamment dans le traitement :
- de l’onchocercose,
- de la strongyloïdose,
- de la filariose lymphatique,
- de la loase,
- de l’ascaridiose,
- de certaines formes de trichuriase,
- de la gnathostomose,
- de la larva migrans cutanée,
- de la gale causée par Sarcoptes scabiei,
- des infestations à Demodex,
- de certaines pédiculoses.
Dans plusieurs régions tropicales, l’administration massive d’ivermectine fait partie des stratégies de santé publique destinées à réduire les maladies transmises par les moustiques ou d’autres vecteurs.
L’ivermectine et son activité anti-inflammatoire
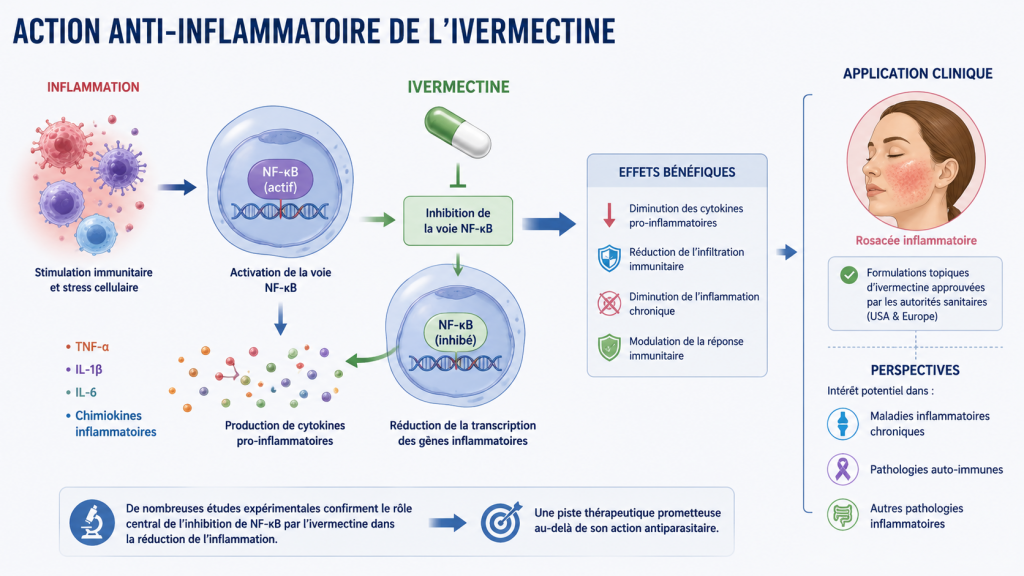
L’un des aspects les plus étudiés ces dernières années concerne les propriétés anti-inflammatoires de l’ivermectine.
Des travaux expérimentaux ont montré que cette molécule peut moduler certaines voies cellulaires impliquées dans l’inflammation chronique. Parmi elles, la voie NF-κB occupe une place centrale.
NF-κB est un facteur de transcription majeur impliqué dans la production de cytokines pro-inflammatoires telles que :
- le TNF-α,
- l’IL-1β,
- l’IL-6,
- diverses chimiokines inflammatoires.
L’inhibition de cette voie pourrait expliquer certains effets bénéfiques observés dans les maladies inflammatoires cutanées, notamment la rosacée.
Cette découverte a conduit les autorités sanitaires américaines et européennes à approuver certaines formulations topiques d’ivermectine pour le traitement de la rosacée inflammatoire.
Des chercheurs explorent désormais l’intérêt potentiel de cette action immunomodulatrice dans d’autres pathologies inflammatoires chroniques et auto-immunes.
Rosacée, inflammation cutanée et microbiote
Dans le cadre de la rosacée, l’ivermectine pourrait agir selon plusieurs mécanismes complémentaires :
- réduction de l’inflammation locale,
- diminution de la charge en Demodex folliculorum,
- modulation immunitaire,
- réduction du stress oxydatif cutané.
Ces observations renforcent l’hypothèse selon laquelle certains déséquilibres du microbiote cutané et certaines réactions inflammatoires excessives jouent un rôle clé dans les maladies dermatologiques chroniques.
Activité antivirale : un domaine encore exploratoire
L’ivermectine a également suscité un intérêt considérable pour ses propriétés antivirales potentielles.
Des études in vitro ont montré qu’elle pouvait perturber le transport intracellulaire de certaines protéines virales en ciblant le système importine α/β1. Ce mécanisme est utilisé par plusieurs virus pour pénétrer dans le noyau cellulaire et détourner les fonctions de la cellule hôte.
Parmi les virus étudiés figurent :
- certains flavivirus,
- les adénovirus,
- le virus de la dengue,
- le virus Zika,
- le SARS-CoV-2.
Toutefois, il est essentiel de souligner que la majorité des résultats observés concernent des études cellulaires en laboratoire. Les concentrations utilisées in vitro ne correspondent pas toujours aux doses cliniquement atteignables chez l’humain.
Ivermectine et adénovirus : des résultats prometteurs en laboratoire
Les adénovirus humains peuvent provoquer des infections sévères chez les personnes immunodéprimées et chez certains enfants fragiles.
Des recherches expérimentales ont montré que l’ivermectine pourrait inhiber plusieurs étapes clés du cycle viral :
- transcription des gènes précoces,
- réplication du génome viral,
- synthèse des protéines virales,
- production de particules infectieuses.
Les chercheurs ont également observé une inhibition dose-dépendante sur certaines souches d’adénovirus humains, notamment HAdV-C5 et HAdV-B3.
Ces travaux suggèrent un potentiel antiviral intéressant, mais des études cliniques humaines restent indispensables avant toute conclusion thérapeutique.
Ivermectine et SARS-CoV-2 : entre espoir scientifique et controverse
Pendant la pandémie de COVID-19, l’ivermectine a été étudiée dans de nombreux pays en raison de ses effets antiviraux observés in vitro.
Certains travaux expérimentaux ont suggéré qu’elle pouvait réduire la réplication virale en perturbant les mécanismes de transport nucléaire nécessaires au virus.
Cependant, les résultats cliniques obtenus chez l’humain sont restés hétérogènes. Plusieurs méta-analyses et essais randomisés ont produit des conclusions contradictoires.
À ce jour, les grandes agences sanitaires internationales considèrent que les preuves restent insuffisantes pour recommander l’ivermectine comme traitement standard du COVID-19 en dehors des protocoles de recherche.
L’ivermectine comme agent anticancéreux potentiel
L’un des domaines les plus fascinants de la recherche actuelle concerne l’activité anticancéreuse potentielle de l’ivermectine.
Depuis 2015, plusieurs équipes scientifiques ont mis en évidence des effets antiprolifératifs sur différentes lignées cellulaires tumorales humaines.
Les mécanismes étudiés incluent :
- induction de l’autophagie,
- stimulation de l’apoptose,
- inhibition de la voie Akt/mTOR,
- modulation du stress oxydatif,
- altération des fonctions mitochondriales,
- inhibition de l’angiogenèse tumorale,
- perturbation du métabolisme énergétique des cellules cancéreuses.
Les cancers étudiés incluent notamment :
- le cancer du sein,
- le cancer du côlon,
- le carcinome hépatocellulaire,
- le cancer de la prostate,
- le cancer du poumon,
- le glioblastome,
- le mélanome,
- certains cancers gynécologiques,
- certaines leucémies.
Il demeure cependant crucial de rappeler que la majorité des données disponibles proviennent d’études précliniques réalisées sur des cellules ou des modèles animaux.
Cancer du sein : inhibition de la voie Akt/mTOR
Le cancer du sein fait partie des cancers les plus étudiés dans le cadre des recherches sur l’ivermectine.
Des travaux expérimentaux ont montré que l’ivermectine pouvait réduire significativement la prolifération de cellules cancéreuses mammaires.
Le mécanisme principal étudié implique la voie Akt/mTOR, essentielle à la croissance et à la survie tumorale.
Akt/mTOR
L’ivermectine favoriserait également la dégradation de PAK1, une kinase impliquée dans le développement de nombreux cancers humains.
Certaines études suggèrent par ailleurs un intérêt potentiel dans les cancers du sein triple négatif, connus pour leur agressivité et leurs options thérapeutiques limitées.
Des chercheurs ont observé que l’ivermectine pourrait influencer :
- la transition épithélio-mésenchymateuse,
- l’expression de l’E-cadhérine,
- certaines résistances hormonales,
- la sensibilité au tamoxifène.
Ces observations demeurent encore expérimentales et nécessitent des essais cliniques robustes.
Glioblastome : apoptose et stress oxydatif
Le glioblastome représente l’une des tumeurs cérébrales les plus agressives.
Des études in vitro ont montré que l’ivermectine pouvait :
- ralentir la prolifération tumorale,
- induire l’apoptose,
- perturber les mitochondries,
- augmenter le stress oxydatif intracellulaire,
- réduire l’angiogenèse.
La voie Akt/mTOR semble également impliquée dans ces mécanismes.
Toutefois, une limite importante concerne la capacité restreinte de l’ivermectine à franchir la barrière hémato-encéphalique, ce qui pourrait limiter son efficacité clinique dans les tumeurs cérébrales humaines.
Sécurité, tolérance et précautions d’emploi
Le profil de sécurité de l’ivermectine est généralement considéré comme favorable chez l’adulte lorsqu’elle est utilisée dans le cadre des indications validées.
Les effets secondaires les plus fréquents incluent :
- nausées,
- vertiges,
- fatigue,
- troubles digestifs,
- réactions cutanées transitoires.
Dans certaines infections parasitaires massives, notamment la loase associée à une forte charge microfilarienne, la destruction rapide des parasites peut provoquer des réactions neurologiques sévères, y compris des encéphalopathies.
Par ailleurs :
- les données chez la femme enceinte restent insuffisantes,
- l’automédication est déconseillée,
- certaines personnes présentant une fragilité hépatique nécessitent une surveillance particulière,
- les interactions médicamenteuses doivent être évaluées au cas par cas.
Une molécule prometteuse nécessitant encore des validations cliniques officielles
L’ivermectine illustre parfaitement comment une molécule ancienne peut révéler progressivement des propriétés biologiques inattendues.
Son activité antiparasitaire est solidement établie depuis plusieurs décennies. En revanche, ses propriétés anti-inflammatoires, antivirales et anticancéreuses restent encore largement exploratoires dans de nombreux domaines, et ce malgré les nombreux témoignages de rémission de cancer an association avec le mebendazole et fenbendazole.
Les résultats précliniques observés dans les études cellulaires et animales ouvrent des perspectives intéressantes, mais ils ne suffisent pas à confirmer une efficacité thérapeutique chez l’humain.
Des essais cliniques rigoureux, randomisés et de grande ampleur restent indispensables afin de déterminer :
- les doses réellement efficaces,
- les mécanismes biologiques exacts,
- les populations pouvant bénéficier du traitement,
- les limites de sécurité à long terme,
- les interactions potentielles avec d’autres thérapies.
L’ivermectine demeure ainsi un sujet majeur de recherche biomédicale moderne, à l’interface entre parasitologie, immunologie, virologie et oncologie.
Ivermectine, mébendazole et fenbendazole : des mécanismes anticancéreux convergents étudiés en recherche expérimentale
L’ivermectine, le mébendazole et le fenbendazole appartiennent à des familles antiparasitaires différentes, mais les recherches expérimentales récentes ont mis en évidence plusieurs similitudes biologiques dans leur manière d’agir sur les cellules tumorales.
Ces trois molécules semblent perturber des mécanismes fondamentaux indispensables à la survie des cellules cancéreuses, ce qui explique l’intérêt croissant pour leur étude en association dans certaines approches expérimentales de type « repositionnement médicamenteux ».
Le mébendazole et le fenbendazole agissent principalement sur les microtubules cellulaires via la liaison à la β-tubuline, provoquant une désorganisation du cytosquelette tumoral.
Cette perturbation bloque la division cellulaire, freine la mitose et peut conduire à l’apoptose des cellules cancéreuses.
L’ivermectine, bien qu’ayant un mécanisme initial différent, semble converger vers des effets similaires en inhibant plusieurs voies de signalisation majeures impliquées dans la prolifération tumorale, notamment Akt/mTOR, WNT/β-caténine et certaines protéines kinases comme PAK1.
Ces trois molécules partagent également une capacité étudiée à induire un stress oxydatif intracellulaire, à perturber les mitochondries tumorales et à stimuler l’autophagie ou l’apoptose programmée des cellules cancéreuses.
Un autre point de convergence observé dans plusieurs modèles précliniques concerne leur impact potentiel sur le métabolisme énergétique tumoral.
Les cellules cancéreuses dépendent fortement du glucose, de la glycolyse et d’une production énergétique dérégulée pour maintenir leur prolifération rapide.
Des travaux suggèrent que le fenbendazole, le mébendazole et l’ivermectine pourraient chacun perturber certains aspects de ce métabolisme anormal, créant un environnement moins favorable à la croissance tumorale.
De plus, ces molécules semblent présenter des effets anti-angiogéniques, réduisant potentiellement la formation de nouveaux vaisseaux sanguins nécessaires à l’alimentation des tumeurs.
Certaines études indiquent également une possible action sur les cellules souches cancéreuses et sur les mécanismes de résistance aux chimiothérapies conventionnelles, notamment via la modulation des pompes d’efflux cellulaire et de certaines voies inflammatoires chroniques comme NF-κB.
Dans les hypothèses de trithérapie expérimentale associant ivermectine, mébendazole et fenbendazole, les chercheurs s’intéressent donc à une éventuelle complémentarité biologique : désorganisation des microtubules, inhibition de la prolifération cellulaire, perturbation mitochondriale, diminution de l’inflammation tumorale, induction de l’apoptose et altération du microenvironnement tumoral.
Toutefois, il est essentiel de souligner que ces approches restent principalement fondées sur des études in vitro, des modèles animaux et des observations précliniques.
Principales références scientifiques sur l’ivermectine, le mébendazole et le fenbendazole dans la recherche anticancéreuse
Références générales sur l’ivermectine et ses effets anticancéreux
- Juarez M, Schcolnik-Cabrera A, Dueñas-Gonzalez A.
The multitargeted drug ivermectin: from an antiparasitic agent to a repositioned cancer drug.
American Journal of Cancer Research. 2018;8(2):317-331. - Dou Q, Chen HN, Wang K, et al.
Ivermectin induces cytostatic autophagy by blocking the PAK1/Akt axis in breast cancer.
Cancer Research. 2016;76(15):4457-4469. - Liu Y, Fang S, Sun Q, et al.
Anthelmintic drug ivermectin inhibits angiogenesis, growth and survival of glioblastoma through inducing mitochondrial dysfunction and oxidative stress.
Biochemical and Biophysical Research Communications. 2016;480(3):415-421. - Gallardo F, Mariamé B, Gence R, et al.
The anthelmintic ivermectin induces chloride-dependent membrane hyperpolarization and cell death in leukemia cells.
Biochemical Pharmacology. 2018;149:10-23. - Melotti A, Mas C, Kuciak M, et al.
The ivermectin-sensitive chloride channel GluClαβ mediates the ability of ivermectin to inhibit WNT-TCF pathway in human cancer.
EMBO Molecular Medicine. 2014;6(10):1263-1278. - Nishio M, Sugimachi K, Goto H, et al.
Dysregulated YAP1/TAZ and TGF-β signaling mediate hepatocarcinogenesis in Mob1a/1b-deficient mice.
Proceedings of the National Academy of Sciences. 2016.
(Études incluant l’ivermectine comme inhibiteur de YAP1)
Références sur le mébendazole dans le cancer
- Bai RY, Staedtke V, Aprhys C, et al.
Antiparasitic mebendazole shows survival benefit in 2 preclinical models of glioblastoma multiforme.
Neuro-Oncology. 2011;13(9):974-982. - Nygren P, Larsson R.
Drug repositioning: new treatment options for cancer and other diseases.
Acta Oncologica. 2014;53(3):353-361. - Dobrosotskaya IY, Hammer GD, Schteingart DE, et al.
Mebendazole monotherapy and long-term disease control in metastatic adrenocortical carcinoma.
Endocrine Practice. 2011;17(3):e59-e62. - Mukhopadhyay T, Sasaki J, Ramesh R, Roth JA.
Mebendazole elicits a potent antitumor effect on human cancer cell lines both in vitro and in vivo.
Clinical Cancer Research. 2002;8(9):2963-2969. - Doudican N, Rodriguez A, Osman I, Orlow SJ.
Mebendazole induces apoptosis via Bcl-2 inactivation in chemoresistant melanoma cells.
Molecular Cancer Research. 2008;6(8):1308-1315. - Pinto LC, Soares BM, Pinheiro JJ, et al.
The anthelmintic drug mebendazole inhibits growth, migration and invasion in gastric cancer cell models.
Molecular Biology Reports. 2015.
Références sur le fenbendazole et les mécanismes tumoraux
- Dogra N, Kumar A, Mukhopadhyay T.
Fenbendazole acts as a moderate microtubule destabilizing agent and causes cancer cell death by modulating multiple cellular pathways.
Scientific Reports. 2018;8:11926. - Gao P, Dang CV.
Cancer cell metabolism and the Warburg effect.
Trends in Biochemical Sciences. 2007.
(Référence importante pour comprendre les hypothèses métaboliques utilisées avec le fenbendazole) - Bai RY, Staedtke V, Wanjiku T, et al.
Brain penetration and efficacy of different mebendazole polymorphs in a mouse brain tumor model.
Clinical Cancer Research. 2015.
(Souvent cité dans les comparaisons fenbendazole/mébendazole) - Kohler P.
The biochemical basis of anthelmintic action and resistance.
International Journal for Parasitology. 2001;31(4):336-345. - Sasaki J, Ramesh R, Chada S, et al.
The anthelmintic drug fenbendazole inhibits microtubule function and glucose uptake in cancer cells.
Études précliniques fréquemment citées dans la littérature expérimentale.
Références sur les voies Akt/mTOR, autophagie et apoptose
- Porta C, Paglino C, Mosca A.
Targeting PI3K/Akt/mTOR signaling in cancer.
Frontiers in Oncology. 2014;4:64. - White E.
The role for autophagy in cancer.
Journal of Clinical Investigation. 2015;125(1):42-46. - Fulda S, Debatin KM.
Extrinsic versus intrinsic apoptosis pathways in anticancer chemotherapy.
Oncogene. 2006;25(34):4798-4811.
Références sur NF-κB et inflammation tumorale
- Karin M.
NF-kappaB as a critical link between inflammation and cancer.
Cold Spring Harbor Perspectives in Biology. 2009;1(5):a000141. - Xia Y, Shen S, Verma IM.
NF-κB, an active player in human cancers.
Cancer Immunology Research. 2014;2(9):823-830.
Références sur les microtubules et la division tumorale
- Jordan MA, Wilson L.
Microtubules as a target for anticancer drugs.
Nature Reviews Cancer. 2004;4(4):253-265. - Dumontet C, Jordan MA.
Microtubule-binding agents: a dynamic field of cancer therapeutics.
Nature Reviews Drug Discovery. 2010;9(10):790-803.
Références sur le repositionnement des antiparasitaires en oncologie
- Pantziarka P, Bouche G, Meheus L, Sukhatme V, Sukhatme VP.
The repurposing drugs in oncology (ReDO) project.
ecancermedicalscience. 2014;8:442. - Pushpakom S, Iorio F, Eyers PA, et al.
Drug repurposing: progress, challenges and recommendations.
Nature Reviews Drug Discovery. 2019;18(1):41-58. - Pantziarka P, Verbaanderd C, Sukhatme V, et al.
ReDO_DB: the repurposing drugs in oncology database.
ecancermedicalscience. 2018;12:886.
Source : https://pmc.ncbi.nlm.nih.gov/articles/PMC11008553
Category: cancer, déparasitage, Fenbendazole, ivermectine, parasites Tags: ivermectine, ivermectine Akt mTOR, ivermectine anti inflammatoire, ivermectine antiviral, ivermectine apoptose, ivermectine autophagie, ivermectine cancer, ivermectine études cliniques, ivermectine glioblastome ivermectine cancer du sein, ivermectine immunomodulation, ivermectine inflammation chronique, ivermectine mécanisme d’action, ivermectine médecine intégrative, ivermectine NF-κB, ivermectine onchocercose, ivermectine parasites, ivermectine recherche scientifique, ivermectine rosacée, ivermectine SARS-CoV-2
Articles récents
- Fenbendazole & Ivermectine – Protocole métabolique inspiré du Dr William MakisProtocole métabolique inspiré du Dr William Makis : analyse scientifique, mécanismes biologiques et place potentielle des oméga-3 enrichis en polyphénols Introduction Depuis plusieurs années, certains médecins et chercheurs explorent le concept de repositionnement thérapeutique en cancérologie. Cette approche consiste à étudier des molécules déjà...
- Ivermectine : un médicament aux multiples facettesIvermectine : un médicament aux multiples facettes entre antiparasitaire, immunomodulation, virologie et recherche anticancéreuse L’ivermectine est aujourd’hui considérée comme l’un des médicaments les plus marquants de la pharmacologie moderne. Découverte dans les années 1970 par le microbiologiste japonais Satoshi Omura et le parasitologue irlandais...
- Le cancer, fenbendazole & Phyto OncologiePlantes et cancer : curcumine, berbérine… protocole naturel efficace Et si le cancer ne se traitait pas avec une seule solution ? Pendant des années, la recherche a tenté d’isoler LA molécule miracle capable de vaincre le cancer. Résultat ?Des milliers d’études, des milliers...
- Fenbendazole et cancer du sein : un potentiel anticancéreuxFenbendazole et cancer du sein : un potentiel anticancéreux via la pyroptose et la glycolyse Une nouvelle piste face à la résistance thérapeutique Le traitement du cancer du sein reste un défi majeur en oncologie moderne. L’une des principales difficultés réside dans la capacité...
- Fenbendazole et cancer : 50 années de brevets oubliésFenbendazole et cancer : 50 ans de recherches, de brevets… et une question qui dérange Et si une molécule oubliée changeait la donne ? Tout commence loin des laboratoires d’oncologie. Le fenbendazole n’a pas été conçu pour traiter le cancer.Il n’a jamais été pensé...
- Fenbendazole et parasites : mécanismesFenbendazole et parasites : mécanismes, efficacité et enjeux biologiques Une molécule issue des benzimidazoles au cœur des stratégies antiparasitaires Le fenbendazole appartient à la famille des benzimidazoles, une classe d’agents antiparasitaires largement utilisée en médecine vétérinaire et étudiée dans différents contextes biologiques. Son intérêt...
- Parasitoses humaines, inflammation chronique de bas gradeParasitoses humaines, inflammation chronique de bas grade et modulation du terrain biologique : revue narrative des données expérimentales et cliniques Résumé Les infections parasitaires humaines, bien que souvent considérées comme rares dans les pays industrialisés, persistent sous des formes chroniques et subcliniques. Parallèlement, l’inflammation...
- Fenbendazole et cancer : un mécanisme multi-cibleFenbendazole et cancer : un mécanisme multi-cible qui intrigue la recherche Initialement utilisé comme antiparasitaire vétérinaire, le fenbendazole attire aujourd’hui l’attention de la recherche en oncologie. Son intérêt repose sur un point clé : sa capacité à agir simultanément sur plusieurs mécanismes fondamentaux des...
- Mode d’action du fenbendazole au niveau cellulaireDepuis plusieurs années, le fenbendazole suscite un intérêt croissant dans le domaine de la recherche en oncologie. Initialement utilisé comme antiparasitaire vétérinaire, ce composé fait aujourd’hui l’objet d’études exploratoires pour ses effets potentiels sur les cellules cancéreuses. Mais que se passe-t-il réellement au cœur...
- Fenbendazole et cancer : le témoignage d’AlexandraFenbendazole et cancer : le témoignage d’Alexandra face à un parcours hors norme Peut-on envisager d’autres pistes face à un cancer métastatique ? Le mot “cancer” bouleverse une vie.Mais lorsqu’il devient métastatique, il impose souvent un sentiment d’urgence, d’impuissance… et de questionnement. Faut-il suivre...
- Fenbendazole et cancer : analyse des témoignages de réussiteFenbendazole et cancer : analyse des témoignages de réussite et des résultats observés Depuis plusieurs années, un médicament antiparasitaire vétérinaire attire une attention croissante dans les communautés de patients atteints de cancer : le fenbendazole. Initialement utilisé pour traiter les infections parasitaires chez les...
- Fenbendazole & Cancer synthèse des cas connusTémoignages de réussite contre le cancer avec le fenbendazole : synthèse des cas et des résultats observés Depuis quelques années, un médicament antiparasitaire vétérinaire relativement méconnu du grand public attire une attention croissante dans les communautés de patients atteints de cancer : le fenbendazole....
- Fenbendazole & Ivermectine par William MakisProtocole Fenbendazole & Ivermectine par le docteur Makis et Joe Tippens 1. Le Florida Cancer Innovation Fund (60 millions de dollars)En septembre 2025, Ron DeSantis et sa femme Casey DeSantis (survivante du cancer) ont annoncé 60 millions de dollars supplémentaires via le Florida Cancer...
- Une piste inattendue en oncologie : le fenbendazole face au cancer avancéIntroduction La recherche contre le cancer explore aujourd’hui des pistes parfois inattendues. Parmi elles figure le fenbendazole, un médicament initialement développé comme antiparasitaire vétérinaire. Depuis plusieurs années, ce composé attire l’attention de certains chercheurs en raison de ses effets observés sur les cellules cancéreuses...
- Fenbendazole et cancer : mécanismes et science émergenteFenbendazole et cancer : mécanismes d’action potentiels et intérêt scientifique émergent Initialement développé comme antiparasitaire vétérinaire, le fenbendazole suscite aujourd’hui un intérêt croissant dans la recherche scientifique pour ses effets potentiels sur les cellules tumorales. Ce composé appartenant à la famille des benzimidazoles agit...
Commentaires
Archives
Copyright © 2026 · All Rights Reserved · Bien Etre Naturel
Theme: Natural Lite by Organic Themes · RSS Feed