Energie Vitalité Santé Naturellement
Fenbendazole et cancer du sein : un potentiel anticancéreux
Fenbendazole et cancer du sein : un potentiel anticancéreux via la pyroptose et la glycolyse
Une nouvelle piste face à la résistance thérapeutique
Le traitement du cancer du sein reste un défi majeur en oncologie moderne. L’une des principales difficultés réside dans la capacité des cellules tumorales à développer des mécanismes complexes de résistance aux traitements conventionnels (Will et al., 2023).
Dans ce contexte, de nouvelles stratégies émergent, notamment autour de la pyroptose, une forme récente de mort cellulaire programmée à fort potentiel thérapeutique (Chen et al., 2022).
Parallèlement, le métabolisme énergétique des cellules cancéreuses, en particulier la glycolyse tumorale, joue un rôle clé dans la progression tumorale et la résistance aux antitumoraux (Aft et al., 2003).
Le fenbendazole (FBZ), connu comme antiparasitaire, suscite aujourd’hui un intérêt croissant pour ses propriétés anticancéreuses (Villar et al., 2007).
Fenbendazole : un antiparasitaire aux propriétés anticancéreuses
Initialement utilisé en médecine vétérinaire, le fenbendazole montre des effets prometteurs dans différents types de cancers.
Action sur le métabolisme tumoral
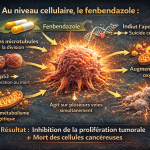
Dans le cancer du poumon non à petites cellules, le FBZ agit sur plusieurs cibles essentielles (Xu et al., 2022) :
- activation du gène suppresseur de tumeur p53
- inhibition du transporteur de glucose GLUT1
- blocage de l’enzyme hexokinase
- diminution de l’absorption du glucose par les cellules cancéreuses
Ces effets perturbent directement la glycolyse, un processus vital pour la survie des cellules tumorales.
Induction de l’apoptose
Le fenbendazole est également capable de déclencher l’apoptose (mort cellulaire programmée classique) :
- dans le cancer colorectal, via des lésions mitochondriales et la voie caspase-3/PARP (Jing et al., 2021)
- dans les cellules sensibles, via l’augmentation de p53
- dans les cellules résistantes au 5-FU, via des mécanismes indépendants de p53 impliquant le fer (Park et al., 2022)
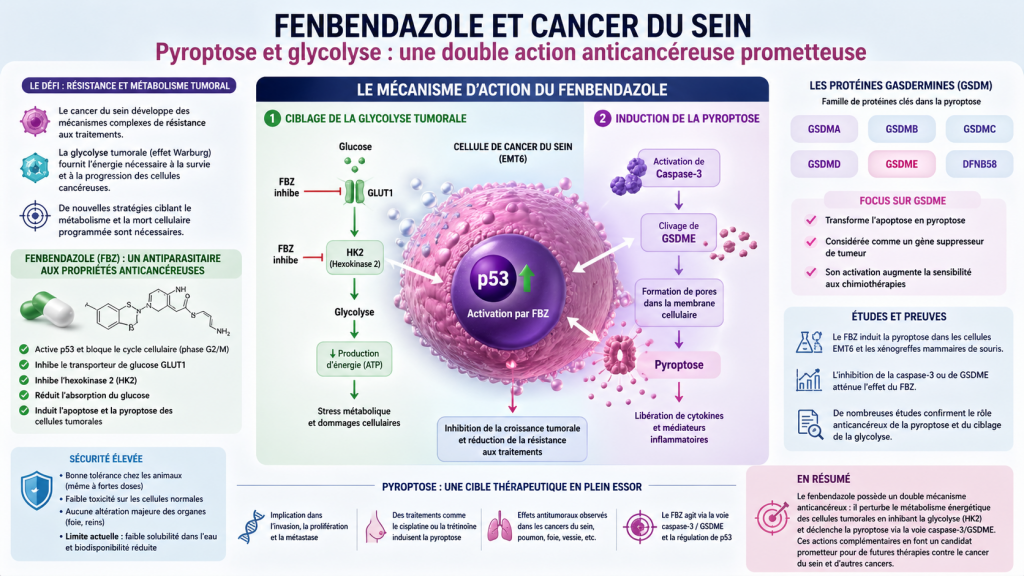
Une découverte majeure : la pyroptose induite par le fenbendazole
Des recherches récentes montrent que le FBZ ne se limite pas à l’apoptose. Il induit également la pyroptose, une forme inflammatoire de mort cellulaire.
Cette action a été observée :
- dans des cellules de cancer du sein (EMT6)
- dans des modèles animaux (xénogreffes mammaires)
Les analyses (viabilité cellulaire, imagerie tumorale, biomarqueurs) confirment clairement ce mécanisme.
Le rôle clé de la voie caspase-3 / GSDME
La pyroptose repose sur l’activation des protéines de la famille des gasdermines.
Contrairement à de nombreux traitements qui activent GSDMD, le fenbendazole agit principalement via :
la voie caspase-3 / GSDME
Pourquoi GSDME est-elle importante ?
- Elle transforme l’apoptose en pyroptose
- Elle est considérée comme un gène suppresseur de tumeur
- Son activation augmente la sensibilité aux chimiothérapies
Plusieurs études confirment son rôle clé :
- inhibition de la croissance tumorale (Lage et al., 2001)
- implication dans le cancer gastrique (Akino et al., 2007)
- conversion de l’apoptose en pyroptose sous chimiothérapie (Wang et al., 2018 ; Jung et al., 2023)
Dans cette étude, l’inhibition de caspase-3 ou de GSDME réduit fortement l’effet du FBZ, confirmant ce mécanisme.
Le rôle central du gène p53
Le gène p53 est impliqué dans plus de 50 % des cancers humains.
Il agit comme un véritable “gardien du génome” :
- blocage du cycle cellulaire
- réparation de l’ADN
- induction de l’apoptose
- inhibition de l’angiogenèse
Le fenbendazole semble stimuler l’expression de p53, renforçant ses effets anticancéreux, notamment via un blocage du cycle cellulaire en phase G2/M (Jung et al., 2023).
Glycolyse et effet Warburg : une cible thérapeutique majeure
Les cellules cancéreuses consomment massivement du glucose, même en présence d’oxygène. Ce phénomène est connu sous le nom d’effet Warburg (Zhu et al., 2022).
L’enzyme clé : HK2
L’hexokinase 2 (HK2) est essentielle à la glycolyse tumorale (Padilla et Lee, 2021).
Plusieurs composés anticancéreux ciblent déjà cette enzyme :
- xanthohumol (Liu et al., 2019)
- tanshinone IIA (Li et al., 2020)
Le fenbendazole agit également sur HK2, perturbant la glycolyse et favorisant la mort des cellules tumorales.
Sécurité et limites du fenbendazole
Un profil de sécurité favorable
Les études montrent :
- une bonne tolérance chez les animaux, même à fortes doses (Muser et Paul, 1984)
- une faible toxicité cellulaire sur les cellules normales
- aucune altération majeure des organes (foie, reins)
Une limite importante : la biodisponibilité
Le principal obstacle reste :
sa faible solubilité dans l’eau
Cela limite son absorption et son efficacité. Des recherches sont en cours pour améliorer ce point.
Pyroptose et thérapies anticancéreuses : un domaine en expansion
De nombreux traitements exploitent désormais la pyroptose :
- le cisplatine dans le cancer du sein triple négatif (Yan et al., 2021)
- la trétinoïne dans les cancers ORL (Cai et al., 2021)
Des études ont également démontré des effets antitumoraux dans :
- cancer du sein
- foie
- poumon
- vessie
(Hou et al., 2020 ; Derangère et al., 2014 ; Lin et al., 2021 ; Zhang et al., 2022)
Conclusion : un double mécanisme prometteur
Le fenbendazole apparaît comme un candidat intéressant en oncologie expérimentale grâce à une double action :
✔ inhibition du métabolisme tumoral (glycolyse via HK2)
✔ induction de la pyroptose (voie caspase-3 / GSDME)
Ces résultats ouvrent la voie à de nouvelles stratégies thérapeutiques, notamment dans les cancers résistants. Etudes sources
Commandez votre Fenbendazole de qualité pur 99% – Cliquez sur l’image ci-dessous
code coupon FENBEN10 remise de 10% immédiate